
科目: 来源: 题型:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目: 来源: 题型:
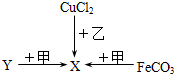 如图所示的三种转化过程都是在水溶液中进行的,但FeCO3和化合物Y都难溶于水.已知X、Y都是只含两种元素的化合物,甲与乙之间可发生置换反应.请你写出化合物Y的化学式
如图所示的三种转化过程都是在水溶液中进行的,但FeCO3和化合物Y都难溶于水.已知X、Y都是只含两种元素的化合物,甲与乙之间可发生置换反应.请你写出化合物Y的化学式查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
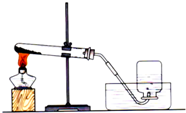 结合“加热高锰酸钾制取氧气”的实验,回答下列问题:
结合“加热高锰酸钾制取氧气”的实验,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
| 实验内容与步骤 | 应得到的实验结果 |
查看答案和解析>>
科目: 来源: 题型:
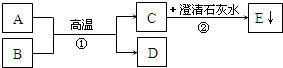 已知A、B为两种黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.
已知A、B为两种黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
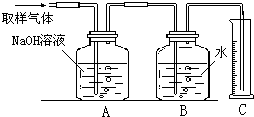
| 总酸性气体体积 |
| 取样总体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com