
科目: 来源: 题型:
| ||
| △ |
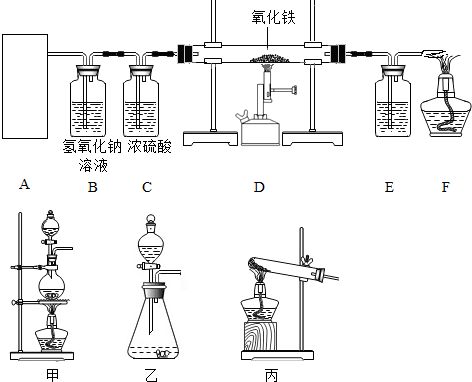
查看答案和解析>>
科目: 来源: 题型:
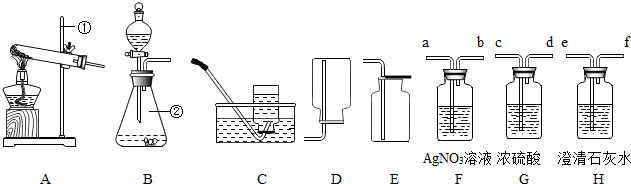
查看答案和解析>>
科目: 来源: 题型:
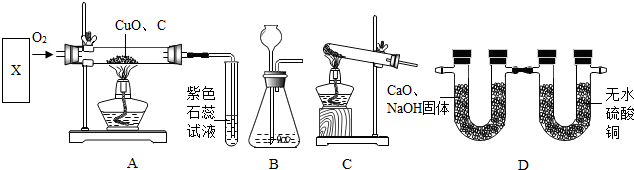
查看答案和解析>>
科目: 来源: 题型:
| 反应时间/分 | 1 | 8 | 13 | 15 | 20 | 25 |
| 实验现象(铝) | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 少量气泡 | 反应停止 |
| 实验现象(铁) | 较多气泡 | 较多气泡 | 较多气泡 | 较多气泡 | 较多气泡 | 少量气泡 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 某初级中学学生为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图1所示)可能是什么物质,大胆猜想并设计实验进行验证.
某初级中学学生为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图1所示)可能是什么物质,大胆猜想并设计实验进行验证.查看答案和解析>>
科目: 来源: 题型:
| 试管编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 碘溶液滴数 | 27 | 24 | 21 | 18 | 15 | 12 | 9 | 6 | 3 | 0 |
| 蒸馏水滴数 | 0 | 3 | 6 | 9 | 12 | 15 | 18 | 21 | 24 | 27 |
| 淀粉溶液滴数 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 |
| 实验步骤 | 可能的实验现象 | 结论 |
双氧水没有完全分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com