
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
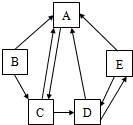 A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):
A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):查看答案和解析>>
科目: 来源: 题型:
| A | O2 | CO2 | H2O | |
| 反应前质量/g | 16 | a | 0 | 0 |
| 反应后质量/g | 0 | 0 | 44 | 36 |
查看答案和解析>>
科目: 来源: 题型:

| ||
| ||
| 操 作 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 组装仪器, | ||
| 装入药品进行加热,打开阀 门 | 观察到 | 则说明有碳酸氢铵存在 |
| 然后打开阀门K2、关闭阀门 K1继续加热 | 最终观察到B中试管内没有气泡冒出,且 | 则说明有碳酸氢钠存在 |
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 装置A中试管质量 | 反应前 | 50.00 |
| 装置A中试管+样品质量 | 反应前 | 70.00 |
| 装置A中试管+固体质量 | 反应后 | 60.60 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 预期现象 | 结论 |
| 步骤1: | 假设2成立 | |
| 步骤2: |
查看答案和解析>>
科目: 来源: 题型:

| 组别 | 样品质量 | CO2的体积 |
| 第1组 | 0.21g | 22.39mL |
| 第2组 | 0.21g | 22.41mL |
| 第3组 | 0.21g | 22.40mL |
查看答案和解析>>
科目: 来源: 题型:
| 次数 | 1 | 2 | 3 | 4 |
| 水的质量(克) | 30.0 | 40.0 | 50.0 | 60.0 |
| 不溶物的质量(克) | 9.1 | 5.4 | 1.7 | 1.7 |
查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入 | 白色沉淀产生 | 该反应的化学方程式: |
| (2)将上述反应后的混合液过滤,取滤液加入 | 证明猜想Ⅱ成立 |

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com