
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

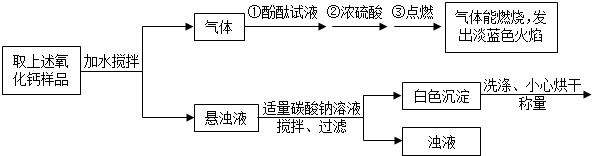
查看答案和解析>>
科目: 来源: 题型:
 同学们在学习了中和反应时,观察到氢氧化钠溶液和稀盐酸反应无明显现象,了解该反应中各种离子的变化情况,进行了如图探究.
同学们在学习了中和反应时,观察到氢氧化钠溶液和稀盐酸反应无明显现象,了解该反应中各种离子的变化情况,进行了如图探究.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
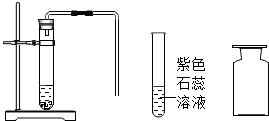 实验可以培养我们创新精神,提高我们的动手能力,请完成以下实验报告的填写.
实验可以培养我们创新精神,提高我们的动手能力,请完成以下实验报告的填写.| 实验步骤 | 实验现象 |
| (1) | |
| (2)装药品,固定装置;往试管中加入固体药品,具体操作为 | 有气泡产生 |
| (3)性质 实验:将气体通入紫色石蕊溶液中 | |
| (4)收集 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com