
科目: 来源: 题型:
 2014年南京青奥会召开在即,以化学的视角来认识青奥会.
2014年南京青奥会召开在即,以化学的视角来认识青奥会.查看答案和解析>>
科目: 来源: 题型:
 铁、铜和铝是人类生活中常用的金属.
铁、铜和铝是人类生活中常用的金属.查看答案和解析>>
科目: 来源: 题型:
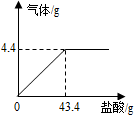 家庭食用面碱(主要成分为碳酸钠)中往往混有少量氯化钠.某课外探究小组的同学为测定食用面碱中碳酸钠的质量分数,设计并进行了以下实验:称取面碱样品11g,全部溶解在50 g水中,向其中加入稀盐酸,至不再生成气泡为止.如图是所加稀盐酸质量与生成气体质量的关系图.请完成下列计算:
家庭食用面碱(主要成分为碳酸钠)中往往混有少量氯化钠.某课外探究小组的同学为测定食用面碱中碳酸钠的质量分数,设计并进行了以下实验:称取面碱样品11g,全部溶解在50 g水中,向其中加入稀盐酸,至不再生成气泡为止.如图是所加稀盐酸质量与生成气体质量的关系图.请完成下列计算:查看答案和解析>>
科目: 来源: 题型:
 随着汽车数量的剧增,解决汽车带来的环境问题已成已经迫在眉睫.请根据要求回答问题:
随着汽车数量的剧增,解决汽车带来的环境问题已成已经迫在眉睫.请根据要求回答问题:查看答案和解析>>
科目: 来源: 题型:
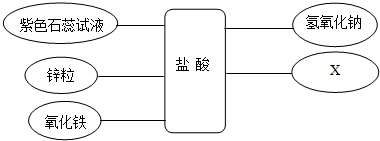
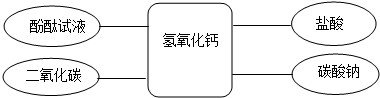
查看答案和解析>>
科目: 来源: 题型:
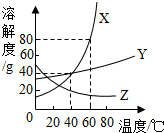 如图是X、Y、Z三种不含结晶水的固体物质的溶解度曲线
如图是X、Y、Z三种不含结晶水的固体物质的溶解度曲线查看答案和解析>>
科目: 来源: 题型:
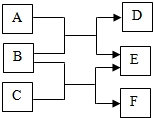 物质A-F都是初中化学中的常见物质,它们有如图所示的转化关系,回答下列问题(反应条件已略):
物质A-F都是初中化学中的常见物质,它们有如图所示的转化关系,回答下列问题(反应条件已略):查看答案和解析>>
科目: 来源: 题型:



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com