
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 序号 | 溶液中的盐 | 固体不溶物的成分 |
| ① | FeCl2、CuCl2、FeCl3 | |
| ② | 无 | |
| ③ | FeCl2、CuCl2 | |
| ④ | Cu | |
| ⑤ | Fe、Cu |
| 组别 | ① | ② | ③ | ④ |
| 混合粉末质量/g | 40 | 40 | 40 | 40 |
| FeCl3溶液体积/mL | 150 | 300 | 330 | 350 |
| 反应后剩余固体质量/g | 23.2 | 6.4 | 2.56 | x |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
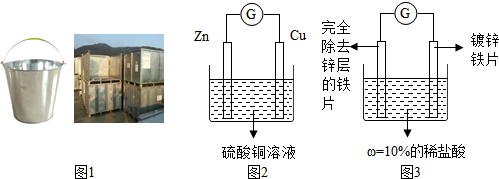
查看答案和解析>>
科目: 来源: 题型:
 A、B、C、D分别是铁、硫酸铜、石灰水、稀盐酸中的一种物质,请回答下列问题:
A、B、C、D分别是铁、硫酸铜、石灰水、稀盐酸中的一种物质,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一: 取该液体适量于试管中,向其中加入少量 |
没有气泡产生. |
该液体不是过氧化氢溶液. |
| 步骤二: 取该液体适量于试管中,向其中滴加少量氯化钡溶液. |
该液体是稀硫酸. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com