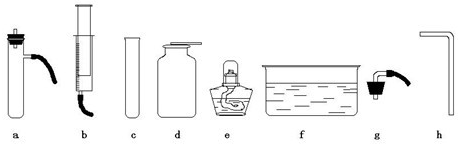
通过初中一年的化学学习,你已经掌握了实验室制取气体的有关规律,如图所示是老师提供的一些实验装置,根据如图1所示回答下列问题:

(1)B装置中仪器甲的名称是
,仪器乙的名称是
;
(2)关闭B装置中的止水夹后,从甲向乙中注入一定量的水,静止后如图所示,则B装置是否漏气?
(填“漏气”、“不漏气”或“无法确定”);
(3)如果实验室用A、E组合来制取并收集氧气,A装置的试管口应添加
;写出实验室用A装置制取氧气的化学方程式
;实验结束时应先
后
.
(4)已知氨气密度小于空气,极易溶于水,具有强烈的刺激性气味,是空气的污染物之一.某校化学研究性学习小组的同学在查阅资料时得知氨气也有还原性.运用类比的思想,既然氨气具有还原性,能否象CO那样还原CuO呢?于是他们设计实验制取氨气并探究上述问题.请你参与该小组的活动并完成下列研究:
(一)制取氨气
①实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式
.
②制取并收集氨气应选用图1中
和
组合(填序号).
(二)性质探究
该小组成员用注射器抽取实验一中生成的未经干燥的氨气,按如图2所示装置进行实验,探究氨气还原性并验证其产物.(夹持装置未画出,碱石灰是NaOH和CaO固体混合物):
③有同学发现该装置在设计上有一定的缺陷,为确保实验结果的准确性,他认为还应该在A、B之间增加一个干燥装置.于是他选择了如图3中的
(填“甲”或“乙”).
④利用改进后的装置进行实验,观察到黑色粉末变为红色物质,无水CuSO
4变蓝,同时生成一种无污染的气体单质.请写出NH
3与CuO反应的化学方程式
.
(三)问题讨论
⑤有同学认为:NH
3与CuO反应生成的红色物质也可能是Cu
2O.
已知氧化亚铜与稀硫酸反应时,能生成CuSO
4和Cu和水.写出氧化亚铜与稀硫酸反应的化学方程式
.
请你设计一个简单的实验检验该红色物质中是否含有Cu
2O.
操作
;
现象
;
结论
.
⑥在解决了上述问题后,又有同学提出:Cu
2O与CuO的热稳定性哪个更强?于是又他们进行了如下实验:取9.8g Cu(OH)
2固体,加热到80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A.冷却后称量,A的质量为7.2g.据此可推得A的化学式为
.(请写出计算过程)根据该实验,同学们得出
在高温下更稳定.


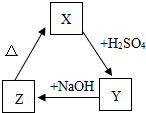 X、Y、Z之间存在如图转化关系:
X、Y、Z之间存在如图转化关系: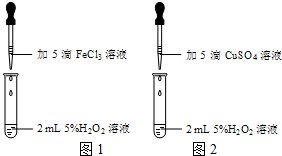 资料表明:有许多金属的盐对双氧水的分解具有催化作用.为比较铁盐和铜盐对H2O2分解的催化效果,某同学设计了如图所示的实验.请回答:
资料表明:有许多金属的盐对双氧水的分解具有催化作用.为比较铁盐和铜盐对H2O2分解的催化效果,某同学设计了如图所示的实验.请回答: