
科目: 来源: 题型:
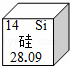
如图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是( )
|
| A. | 该元素原子的质子数为14 | B. | 该元素一个原子的核外有14个电子 |
|
| C. | 该元素属于非金属元素 | D. | 该元素的相对原子质量为28.09克 |
查看答案和解析>>
科目: 来源: 题型:
学会分析,寻找规律是学好化学的方法之一.分析NaCl、X、HClO、KClO3、KClO4的排列顺序规律,可知X代表的物质是( )
|
| A. | HCl | B. | Ca(ClO)2 | C. | Cl2 | D. | Cl2O |
查看答案和解析>>
科目: 来源: 题型:
有关水的电解实验,下列说法正确的是( )
|
| A. | 与电源正级相连的一端产生的气体能燃烧 |
|
| B. | 证明水是由氢气和氧气组成的 |
|
| C. | 正、负二极产生气体的质量比为1:2 |
|
| D. | 证明水是由氢元素和氧元素组成的 |
查看答案和解析>>
科目: 来源: 题型:
小明同学决定用氯酸钾制取氧气。他取了5克的氯酸钾(内含少量杂质不参与反应)与1克二氧化锰混合后,依次加热该混合物t1,t2,t3,t4时间后,分别冷却称量剩余固体,记录的有关数据如下表。试根据下表回答:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(克) | 4.24 | 4.16 | 4.08 | 4.08 |
(1)加热 时间后,氯酸钾已完全反应;
(2)完全反应后,理论上最多产生氧气的质量为 g;物质的量为 mol
(3)若有0.1mol纯氯酸钾,可制得氧气多少mol?(在答题纸的方框内写出计算过程)
|
查看答案和解析>>
科目: 来源: 题型:
在“空气中氧气含量的测定”实验探究中,
(1)甲同学设计了如图1的实验方案:在集气瓶内放足量红磷,
塞紧橡皮塞,用放大镜聚集太阳光来引燃红磷,待红磷火焰熄灭
且集气瓶冷却至室温后,打开止水夹。如果实验成功,那实验过程中观察
到的主要现象有 。
(2) 乙同学设计了如图2的实验方案:将足量镁粉点燃后放入钟罩装置进行实验,写出镁粉与氧气反应的化学方程式 。
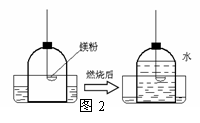 燃烧完毕冷却后水几乎占满整个钟罩,已知镁是一种很活泼的金属,请推测产生这一现象的可能原因 。
燃烧完毕冷却后水几乎占满整个钟罩,已知镁是一种很活泼的金属,请推测产生这一现象的可能原因 。
 将图2中镁粉换成炭粉进行相同实验不能测定空气中氧气的含量
将图2中镁粉换成炭粉进行相同实验不能测定空气中氧气的含量
其原因是 。
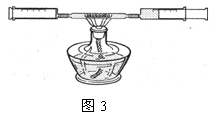
(3)丙同学设计了如图3的实验方案:反应容器是由两个针筒
和中间的玻璃管组成的密闭系统,容器内留有30mL空气。加热
到铜丝的温度升高后,交替缓缓推动两个注射器活塞,观察到亮红色
 的铜丝表面覆盖着一层黑色物质(反应方程式:2Cu+O2 2CuO),实验数据记录如下:
的铜丝表面覆盖着一层黑色物质(反应方程式:2Cu+O2 2CuO),实验数据记录如下:
| 反应前容器内空气体积 | 反应后容器内气体体积 |
| 30mL | X mL |
I.反应后容器内气体体积X理论上为 mL。
II.如果反应结束后测得容器内气体体积为28mL,假设装置气密性完好,那造成实验有误差的原因可能是 (试举一个即可)。
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组为了选择实验室制取二氧化碳的原料,对影响盐酸与大理石(大理石中杂质不与盐酸反应)反应的速率快慢的因素展开探究。
提出假设:盐酸与大理石反应的速率快慢与所用HCl的质量分数、大理石颗粒大小有关。
实验设计与实施:
| 实验编号 | 温度 | 5克大理石(碳酸钙纯度相同)规格 | 20克HCl的质量分数 | 完全反应所需时间/s |
| 实验① | 20℃ | 粗颗粒 | 20% | 140 |
| 实验② | 20℃ | 粗颗粒 | 10% | 220 |
| 实验③ | 20℃ | 细颗粒 | 20% | 30 |
根据以上信息回答下列问题:
(1)写出上述实验中反应的化学方程式 。
(2)实验①与②的目的是为了探究 。
(3)实验 和 (填实验编号)的目的是为了探究大理石颗粒粗、细对反应快慢的影响。
你得出的实验结论是 。
(4)拓展与反思:还有哪些因素可能影响该反应的速率快慢呢?
请写出你的一个猜想 ,
实验设计:
 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com