
科目: 来源: 题型:
如果将100 g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为( )
A.50 g B.90 g C.100 g D.200 g
查看答案和解析>>
科目: 来源: 题型:
向100 g 10%的NaOH溶液中加入12.5 g NaOH固体,完全溶解后,所得溶液中溶质质量分数为( )
A.12.5% B.20% C.22.5% D.25%
查看答案和解析>>
科目: 来源: 题型:
冬天,人们常用甘油溶液护肤,使皮肤保持湿润,质量分数为80%的甘油溶液护肤效果最佳。配制80%的甘油溶液500 g,所需甘油的质量为( )
A.80 g  B.40 g
B.40 g
C.400 g D.100 g
查看答案和解析>>
科目: 来源: 题型:
现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是( )
A.m质∶m剂=1∶10 B.m质∶m液=1∶10
C.m质∶m液=1∶11 D.m剂∶m液=10∶11
查看答案和解析>>
科目: 来源: 题型:
某同学完成碳还原氧化铜的实验后,得到亮红色的Cu和暗红色的Cu2O的混合物。现将8.4 g该混合物放入烧杯中,加入过量稀硫酸充分反应后,过滤、洗涤、干燥,得到6.4 g固体。计算原混合物中Cu2O的质量。
 已知:Cu2
已知:Cu2 O + H2SO4 CuSO4 + Cu + H2O
O + H2SO4 CuSO4 + Cu + H2O
查看答案和解析>>
科目: 来源: 题型:
钛(Ti)是广泛应用于航空、航海等领域的一种重要金属。可利用如下反应制得:TiCl4 + 2Mg  Ti + 2MgCl2。现有24 kg镁,计算生成钛的质量。
Ti + 2MgCl2。现有24 kg镁,计算生成钛的质量。
查看答案和解析>>
科目: 来源: 题型:
为验证某碳酸钙样品的纯度为98%(样品中的杂质与稀盐酸不反应),小组同学设计如下两个实验。
【查阅资料】
①无水CaCl2可作干燥剂
 ②2NaOH + CO2 Na2CO3 + H2O
②2NaOH + CO2 Na2CO3 + H2O
【进行实验】
实验均取10.0 g碳酸钙样品和等体积、等浓度的稀盐酸。
| 序号 | 实验装置 | 主要实验步骤 | 实验结果 | ||||||
|
|
    | ①读取反应前电子天平的示数(m1) ②将过量的稀盐酸全部倒入烧杯中 ③待反应停止后,立即读取电子天平的示数(m2) | 测得样品纯度的平均值为93.8% | ||||||
| 实验2 |
| ①在气密性良好的装置中装入药品 ②称量反应前烧杯和烧杯中液体的质量(m3) ③迅速加入过量的稀盐酸 ④待反应停止后,立即称量烧杯和烧杯中液体的质量(m4) | 测得样品纯度的平均值为25.0% |
【解释与结论】
(1)实验1中,判断反应停止的依据是______,反应的化学方程式是______,
造成m2 < m1的主要原因是______。
(2)实验2中测得的样品纯度小于98%的原因可能是______(填序号)。
A.碳酸钙没有完全反应 B.排出的CO2没有完全被NaOH溶液吸收
C.反应容器中CO2有残留 D.NaOH溶液吸收了空气中的CO2
【反思与改进】
 为提高测量结果的准确性,对实验1装置进行改进(如下图所示),测得样品纯度的平均值为97.6%。
为提高测量结果的准确性,对实验1装置进行改进(如下图所示),测得样品纯度的平均值为97.6%。
(1)反应前后,两次称量整个装置及药品的总质量。在第二次
称量前,应该进行的操作是______。
(2)装置中的“无水CaCl2”能提高测量结果的准确性,其原因
是______。
查看答案和解析>>
科目: 来源: 题型:
用如图所示装置(夹持装置已略去)分别进行实验。
 |
(1)用装置A制备氧气。分液漏斗中盛放的药品是______,反应的化学方程式是______。验证所得的气体是氧气的操作是______。
(2)用装置B进行性质实验。注入稀盐酸,试管内反应的化学方程式是______。整个
实验过程中,试管内产生大量气泡,固体减小,还能观察到的实验现象是______。
查看答案和解析>>
科目: 来源: 题型:
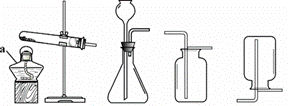
根据下图回答问题。
 | |||||
 | |||||
 | |||||
A B C D E F
(1)仪器a的名称是______。
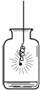
(2)实验室用高锰酸钾制取氧气的化学方程式是______,选用的收集装 置是______
置是______
(填序号,下同)。如图E所示,铁丝与氧气反应的化学方程式是______。
(3)实验室用大理石和稀盐酸制取二氧化碳选用的发生装置是______。如图F所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com