
科目: 来源: 题型:
设计实验:在蜡烛火焰上方罩上一个冷而干燥的烧杯,观察烧杯壁上的现象;再将烧杯迅速倒置,向其中加入少量澄清石灰水,振荡,观察现象。
对上述实验设计思路的描述有以下几点:
①将烧杯罩在火焰上方有利于燃烧产物的汇集;
②用冷的烧杯可使变化过程中产生的水迅速凝结;
③将烧杯迅速倒置可避免产生的气体向空气中散逸;
④振荡有利于产生的气体与石灰水充分接触。
对描述的认识正确的是 ( )
A.①②正确③④错误
B.③④正确①②错误
C.①②③正确④错误
D.①②③④都正确
查看答案和解析>>
科目: 来源: 题型:
人类对原子结构的认识是逐渐深入的。如下是不同时期科学家提出的原子结构模型。
1808年,科学家道尔顿提出了原子论。他认为物质都是由原子直接构成的;原子是一个实心球体,不可再分割。
1897年,英国科学家汤姆森发现原子中存在电子,电子的发现使人们认识到原子是由更小的粒子构成的。1904年汤姆森提出了一个被称为“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中,此模型也被称为“葡萄干布丁”模型。
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大 多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成的。
多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成的。
根据以上材料,请回答:
(1)道尔顿提出了原子论,汤姆森发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照目前初中阶段你学的原子结构的理论,你认为
①道尔顿的原子论存在的缺陷是_____________________________;
②汤姆森原子结构模型的缺陷是______________________________;
(2)根据卢瑟福的实验所产生的现象,不能够获得的结论是________;
A.原子核体积很小 B.原子核质量较大
C.原子核带有正电 D.核外电子带有负电
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想?_________。
查看答案和解析>>
科目: 来源: 题型:
【情景提供】19世纪以前,人们一直以为原子是不可分的,直到1897年,汤姆 森发现了带负电的电子后,才引起人们对原子结构模型的探索。
森发现了带负电的电子后,才引起人们对原子结构模型的探索。
【提出问题】电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?
【进行实验】1911年 英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图:
英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图:
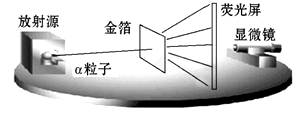
【收集证据】通过显微镜360度转动,观察闪光可观察到绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)若原子质量、正电荷在原子内均匀分布,则极少数α粒子就 (填“会”或“不会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是 。
(2)1μm金箔包含了3 000层金原子,绝大多数α粒子穿过后方向不变,说明 __________________________。
A.原子的质量是均匀分布的
B.原子内部绝大部分空间是空的
(3)科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为以下的 ___________。
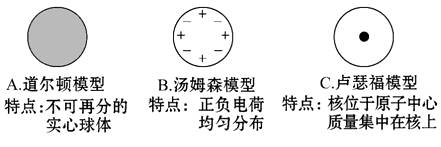
查看答案和解析>>
科目: 来源: 题型:
(1)金属铁是由______(填“原子”“分子”或“离子”,下同)构成的,硫酸铜是由______构成的。
(2)原子得到或失去电子后形成离子。某离子的结构示意图为:
①当a=________时,该粒子是原子;
②当a=8时,该粒子是________(填“原子”“阳离子”或 “阴离子”),其符号为________。
(3)氯化氢是一种无色、有刺激性气味的气体。小明走进实验室就闻到了这种气味,从分子的角度解释这种现象: _________________________。
查看答案和解析>>
科目: 来源: 题型:
稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土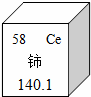 元素,下列有关说
元素,下列有关说 法错误的是( )
法错误的是( )
A.铈的原子序数是58 B.铈属于非金属元素
C.铈原子中的质子数是58 D.铈的相对原子质量是140.1
查看答案和解析>>
科目: 来源: 题型:
近来中国部分地区出现镉污染的大米,食用后对人体有害。根据右图判 断下列有关镉的说法中正确的是( )
A.镉的中子数是48 B.镉属于非金属元素
C.镉的元素符号是Cd D.
查看答案和解析>>
科目: 来源: 题型:
据报道,上海某医院正在研究用放射性碘治疗肿瘤。这种碘原子的核电荷数为53,相对 原子质量为125。下列关于这种原子的说法中,错误的是( )。
原子质量为125。下列关于这种原子的说法中,错误的是( )。
A、 中子数为72 B、 质子数为72
C、 电子数为53 D、质子数和中子数之和为125
查看答案和解析>>
科目: 来源: 题型:
人体中必需的微量元素有铁、氟、锌、硒(Se)、碘等,虽然含量少,但对健康至关重要.下面提供几种微量元素的相关信息,请认真分析并回答下列问题:
①上述微量元素的原子中质子数最少的是 (填元素符号).
②铁离子核外电子数为 .
③硒原子在化学反应中容易得到 个电子,形成硒离子 (填离子符号).
④碘元素的化学性质与氟相似,由此可以推知碘原子最外层电子数为
⑤从B图中你可以获得的信息是 .(写一条)
查看答案和解析>>
科目: 来源: 题型:
有A、B、C、D四种原子,已知它们的核电荷数依次增大且为四个连续的数。B和D的原子核里质子数和中子数相等, A和C的原子核里质子数比中子数少1,已知B原子核外有10个电子。
(1)根据以上事实填写下表:
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 核电荷数 |
| A | ||||
| B |
| |||
| C | ||||
| D |
(2)分析表中的数据,你发现了哪些规律?
①
②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com