
科目: 来源: 题型:
如图所示,某实验小组进行以下实验:

(1)上述实验进行对比的目的是____。
(2)实验后,将A、B两试管中的溶液倒入同一个洁净的烧杯中,溶液无色。再向其中加入一定量的碳酸钠溶液(提示:
CaCl2+Na2CO3=CaCO3↓+2NaCl),所得混合物中溶液的溶质成分有四种情况,请补充完整(酚酞省略不写):①NaCl;②____;③____;④____。若该混合物中溶液无色,选用一种试剂即可确定溶质成分是哪种情况,写出所加试剂,预期现象和结论。
查看答案和解析>>
科目: 来源: 题型:
厨房中有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种。小明对白色粉末的成分进行了探究。
[查阅资料]碳酸钠俗称 ▲ 、苏打,碳酸氢钠俗称小苏打,两者都属于 ▲ (选填“酸”、“碱”、“盐”),都能溶于水,且水溶液都呈碱性。
[实验探究]小明取适量白色粉末,配制成溶液,按表中所示实验方案进行探究。
| 实验步骤 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是 ▲ |
| 2 | 取少量溶液,滴加稀盐酸 | ▲ | |
| 3 | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 |
(1)请完成表中空格。
(2)实验步骤2中可能发生反应的化学方程式为 ▲ (写出一个即可)。实验步骤
3中白色沉淀的成分是 ▲ (填写化学式)。
[实验反思]小明实验后发现上述实验方案并不能确定白色粉末的组成。经老师指导后,小明再取少量配制的溶液滴加氯化钙溶液,没有观察到明显现象,则该白色粉末是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
某同学家中有一袋化肥,可能混入了其它化肥,且化肥包装袋上字迹模糊。该同学进行了以下探究,请你参与探究并填空:
【提出问题】该化肥中含有什么物质?
【收集信息】经询问得知,该化肥可能为铵态氮肥。
【提出猜想】该化肥所含的阴离子可能是Cl-、CO32-、SO42-中的一种或几种。
【实验、记录与分析】
【实验、记录与分析】
| 实验操作步骤 | 实验现象 | 实验分析 |
| (1)取少量该化肥样品和少量熟石灰放在研钵中混合研磨,观察现象 | ① | 含有铵根离子 |
| (2)另取少量该化肥样品于试管中,加入适量的水完全溶解,滴加足量的硝酸钡溶液,再滴加少量稀硝酸,观察 | 无沉淀 | 没有 ② 存在 |
| (3)取(2)所得滤液少量于试管中,滴加 硝酸银溶液,观察 | ③ | 有Cl-存在 |
【实验结论】若该化肥中只含有一种阳离子,则其中一定含有的物质是(写化学式):④ 。
写出步骤③的化学方程式 ⑤ 。
查看答案和解析>>
科目: 来源: 题型:
一次实验课上,细心的小红、小敏同学同时发现盛NaOH 溶液的试剂瓶塞外有少量白色粉末。
【提出问题】白色粉末是什么呢?
【猜想与假设】①白色粉末是NaOH固体
②白色粉未是Na2CO3固体
 ③白色粉未是NaOH和Na2CO3的固体混合物
③白色粉未是NaOH和Na2CO3的固体混合物
【实验探究】为了探究上述猜想。小红、小敏取白色粉未置于烧杯中,加入水配制成溶液。
(1)小红取溶液少量于试管中,加入稀盐酸,有气泡产生,该实验说明猜想
____________不成立。(填序号)
(2)能否向溶液中滴加酚酞试液来证明上述猜想_______________(填“能”或“不能”),你的理由是_______________________________________。
(3)为了探究另两个猜想哪个成立。小敏取溶液少最于试管中,加入过量CaCl2溶液后溶液变浑浊,该反应的化学方程式:__________________________________。过滤,在滤液中滴加酚酞试液变红,表明猜想③成立。
(4) 用化学方程式解释NaOH变质的原因____________________________________,该事实说明NaOH溶液或固体都必须密封保存。
查看答案和解析>>
科目: 来源: 题型:
小明同学欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸钙反应”为研究对象,设计的实验装罝如图所示。
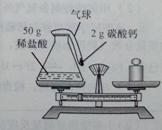
(1)根据实验目的,小明应该测量的数据是_____________________反应前、后(填“只有反应前”“只有反应后”“反应前、后”之一)整个反应装罝(包括锥形瓶、气球和药品)的质量。
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据。
②将碳酸钙粉末全部倒入锥形瓶中,观察到锥形瓶中液体里出现的现象之一是 _________,发生反应的化学方程式是 _____________。
③当反应结束时,气球已经完全鼓起,小明发现天平的指针巳经向右偏了。小明又重新称量,记录了数据。
他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?你认为出现该实验现象的合理解释最应该是下列各项中的 ______________(填序号)。
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律
查看答案和解析>>
科目: 来源: 题型:
下列是初中化学中的一些重要实验,请回答

(1)A是氢气或甲烷的燃烧实验,点燃前必须____________
(2)B实验中能够说明盐酸与氢氧化钠发生了反应的现象是________________________
(3)C是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是____________
(4)D是用碳酸钠粉末与稀盐酸反应制取二氧化碳的简易装置,此装置的最大优点是________________________________________________
查看答案和解析>>
科目: 来源: 题型:
一种名为“污渍爆炸盐”的洗涤产品能高效去除衣物上的顽固污渍,某校化学研究性学习小组的同学在老师的指导下对该产品开展了以下探究活动。
【查阅资料】
“污渍爆炸盐”的主要成分是过碳酸钠(相对分子质量为122),它是一种白色固体粉末,易溶于水且能与水反应生成一种碳酸盐和一种强氧化性的物质,是当前使用最为广泛的洗涤助剂之一。
【实验探究一】过碳酸钠的化学组成
为探究过碳酸钠的化学组成,同学们设计了以下实验,请按要求完成表格内容:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 |
。 |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡产生 |
|
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是 ;过碳酸钠溶于水能生成 (填化学式)。 |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色沉淀 | 反应的化学方程式 。 |
| 实验 小结 | 过碳酸钠的化学式是 ; 过碳酸钠与水反应的化学方程式是 。 |
【实验探究二】:过碳酸钠含量测定
老师给同学们一份含碳酸钠杂质的过碳酸钠样品(不含其它杂质),要求设计方案测定该样品中过碳酸钠的含量,同学们经讨论设计了如下图所示的实验装置。图中装置B盛装氢氧化钠溶液、C盛装澄清石灰水、D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气)。
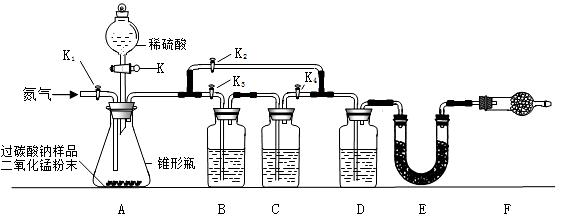
(1)首先关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气排出锥形瓶中的空气,此时装置B的作用是 ;
(2)依次关闭活塞K1、K3、K4,打开活塞K2、K,此时锥形瓶中反应生成的气体是 ,E中装入碱石灰的作用是 ,反应完全后关闭活塞K,再次打开活塞K1通入氮气的作用是 ;
(3)同学们根据E装置在测定前后的质量差计算出了样品中过碳酸钠的含量。装置F的作用是 ,如不连接装置F,测定的过碳酸钠含量会 (填“偏高”或“偏低”)。
查看答案和解析>>
科目: 来源: 题型:
下图是甲同学设计的证明H2和CO具有还原性的实验装置

请回答:
(1)在实验过程中,装置B处能观察到的现象是 ,装置C处发生反应的化学方程式是 ;
(2)乙同学提出甲同学设计太复杂,可将酒精灯合二为一,去掉D处酒精灯而将尾气导管口旋转到A处酒精灯火焰上方即可,请问乙同学的设计是否合理? (填“合理”或“不合理”),理由是 ;
(3)丙同学质疑使澄清石灰水变浑浊的不一定为CO2,也有可能是H2和CO,因此他认为H2和CO在与CuO反应之前应先通过澄清石灰水以验证H2、CO是否能使澄清石灰水变浑浊。你认为丙的设计 (填“必要”或“不必要”),理由是 。
查看答案和解析>>
科目: 来源: 题型:
乙炔(化学式为C2H2)是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成多种化合物。乙炔气体和氧气反应能产生高温火焰(氧炔焰),工人师傅常用氧炔焰切割或焊接金属构件。现在让我们一起对乙炔燃烧(氧炔焰) 的产物进行探究。
的产物进行探究。
【查阅资料】当还原性气体中混有水蒸汽时,则难以还原氧化铜。
【提出问题】乙炔燃烧的产物中除水外主要还有哪些物质?
【假设与猜想】猜想:①一定有______;②可能有一氧化碳。
【实验设计】根据上述两种物质的猜想设计如下实验:
(1)在氧炔焰上方罩一个内壁附着有_____的大烧杯,观察现象。
(2)将乙炔燃烧的产物依次通入足量的澄清石灰水和足量的浓硫酸,将剩余气体通过炽热的氧化铜,若氧化铜变红,说明有(填写化学式)____。
【证据与结论】
实验(1):观察到烧杯内壁附着的____,则猜想①成立。反应的化学方程式为:_____。
实验(2):若氧化铜变红,则猜想②成立。
【分析与交流】实验(2)时,若将乙炔燃烧的产物依次通入足量的浓硫酸和足量的澄清石灰水,再将剩余气体通过炽热的氧化铜,此时氧化铜不变红,能否证明猜想②不成立?____(填“能”或“不能”)。
查看答案和解析>>
科目: 来源: 题型:
在电视上的寻宝或探索节目中,常常看到一些铜制文物上有绿色的锈迹,又称铜绿。某学习小组对铜绿产生了浓厚兴趣。
【提出问题】铜绿中除铜元素外还有其它什么元素?
【查阅资料】①无水硫酸铜遇水变蓝;②碳与一般的酸不反应。
【实验探究】该小组同学找到了一些铜绿并进行了如下实验:
 |
【记录分析】I处绿色物质变黑;
II处无水硫酸铜变蓝;
III处澄清石灰水变浑浊,该处反应的化学方程式为 57 。
【实验结论】铜绿中除铜元素外还有 58 、 59 和碳等元素。
【交流讨论】根据铜绿的组成,小组同学对I处产生的黑色物质的成分有如下两种不 同的猜想:(1)CuO (2)CuO和C的混合物
同的猜想:(1)CuO (2)CuO和C的混合物
【继续探究】取I处冷却后的少量黑色固体于试管中,滴入足量的 60 ,若现象为: 61 ,则证明猜想(1)正确。
【拓展应用】根据铜绿中所含元素,可知铜生锈不仅与空气中的氧气、水有关,还可能与空气中的 62 等有关;要保护博物馆里的青铜器,减缓生锈,我们可以减少青铜器与 63 接触。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com