
科目: 来源: 题型:
三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。
(1)小敏的方法可用如下流程表示,测得的碳酸钙质量分数为_____________;他在过滤操作中,需要用到的玻璃仪器有_______________(选填序号)。
A.酒精灯、漏斗、玻璃棒 B.漏斗、玻璃棒、烧杯 C.酒精灯、试管、玻璃棒
(2)小华取10克样品,用如图甲实验装置进行实验,反应结束后,测得B装置质量增加了4.6克,算得碳酸钙的质量分数,发现与事实严重不符,造成这种情况的可能原因是________________________________________________________。
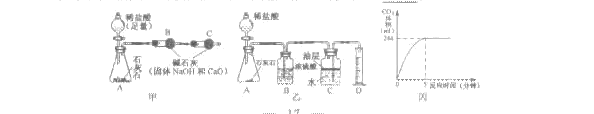
(3)小军用如图乙的实验装置进行实验,将20克稀盐酸加入到1.25克样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8克/升。求该石灰石样品中CaCO3的质量分数。
(4)求实验所用的稀盐酸的溶质质量分数。
查看答案和解析>>
科目: 来源: 题型:
实验后的废液一般需回收处理,不能直接倒入排污管。小科实验后收集到含有碳酸钠和氧氧化钠的混合废液10.22g,他向废液中缓缓滴入溶质质量分数为19.6%的稀硫酸,生成二氧化碳质量与滴入稀硫酸质量的关系如图所示。当废液恰好处理完毕时,溶液总质量为20g。溶于水的气体忽略不计,则

(1)废液恰好处理完毕时,溶液的pH为 。
(2)图中m= g。
(3)废液恰好处理完毕时,回收所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目: 来源: 题型:
下图表示金属活动性顺序中铜、铁和铝被人类大规模开发、利用的大致年限。

(1)分析改图的规律,你认为金属被大规模开发、利用的先后顺序主要与 有关。
(2)科学小组的同学对模拟湿法炼铜实验中得到的铁、铜固体混合物进行含量测定,称取10克固体混合物置于烧杯中,滴加一定质量分数的稀硫酸溶液,记录并绘制了如图所示的曲线。
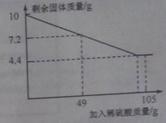
①10克固体混合物中铜的质量为 克;
②所用稀硫酸溶液溶质的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
某同学家的下水管道堵塞了,于是他买了一瓶“管道疏通剂”(部分说明如图)。疏通剂是利用铝与氢氧化钠溶液反应时放出大量的热,以加快氢氧化钠与毛发等淤积物的作用,反应的原理为:2Al+2NaOH+2 H2 O=2NaAlO2+3 H2↑。请回答下列有关问题:
(1)该管道疏通剂需要密封保存的原因是__________________。
(2〕按照使用说明,该同学对“疏通剂”作了进一步研究。先向烧杯中加入206g水,再加入本品200g,当铝粉全部反应后,求:(计算结果保留1位小数)
①生成氢气的体积.(氢气的密度为0.09g/L)
②反应后溶液中氢氧化钠的质量分数。

查看答案和解析>>
科目: 来源: 题型:
2013年5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30克邻叔丁基苯酚完全燃烧,生成88克CO2和25.2克H2O(无其他产物)。已知邻叔丁基苯酚的相对分子质量为150,求:
(1)30克邻叔丁基苯酚中含碳元素 ▲ 克,氢元素 ▲ 克。
(2)邻叔丁基苯酚的化学式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
实验室有瓶标签模糊的烧碱溶液,小军测量其溶质质量分数的操作如下:
①取一洁净的锥形瓶称量,其质量为25.5g,往其中注入一定量上述烧碱溶液,并滴入1滴酚酞溶液后,又称量锥形瓶,质量为37.5g;
②取质量分数为24.5%的稀硫酸逐滴滴入上述锥形瓶中,边滴边振荡,当观察到溶液由红色变为无色时,停止滴液。再次称量锥形瓶,质 量为51.0g
量为51.0g
请解答下列问题:
(1)所取烧碱溶液的质量 = g。(注:滴人酚酞的质量忽略不计)
(2)反应所消耗的稀硫酸质量= g。
(3)通过计算确定该瓶烧碱溶液的溶质质量分数。(列出计算过程)
(4)问题讨论:小亮做同样的实验得到的结果与小军的结果有差异。于是小亮测自己实验后锥形瓶内溶液的pH,pH =6.2,则小亮的结果比小军的 (选填“偏大 ”或“偏小”或“无影响”),原因是 。
”或“偏小”或“无影响”),原因是 。
查看答案和解析>>
科目: 来源: 题型:
乙醇俗称酒精,其化学式为C2H5OH,乙醇中碳、氢、氧三种元素的质最比_____;乙醇中碳元素的质量分数为___________(精确到0.1%);92g乙醇中含碳元素的质量_________________g。
查看答案和解析>>
科目: 来源: 题型:
实验室用大理石与稀盐酸反应制取C02,反应后所得溶
液体积为40 mL(假设大理石中的杂质不与盐酸反应,反应
前后溶液体积不变)。向该溶液中匀速逐滴加入Na2C03溶液
并不断搅拌,测得溶液的pH随时间变化如图所示,该过程
共放出气体660 mL(密度为2.0 g/L),析出沉淀5.090
(1) 根据图像可以看出,Na2C03首先与溶液中的 反应。
(2)本实验制取CO2所用大理石中含CaC03 g。
(3)已知制取C02所用稀盐酸的密度为1.06 g/cm3,求这种盐酸的质量分数。(计算结果保留1位小数,无计算过程不给分)
查看答案和解析>>
科目: 来源: 题型:
守恒思想是化学中重要的学科思想.电荷守恒便是其中之一:电荷守恒是指溶液
中所有的阳离子所带正电荷之和等于所有阴离子所带负电荷之和:例如:某Na2SO4溶液中有X个Na+、y个SO42-则该溶液电荷守恒可表示为x=2y。现有一混合溶液,组成如下表所示,回答下列问题:
| 离子 | K+ | Mg2+ | Cl- | SO42- |
| 个数 | a | b | c | d |
(1)该混合溶液的电荷守恒可表示为: (用a、b、c、d表示)
(2)若该溶液中有两种溶质,这两种溶质可以是KCl和MgSO4,也可以是 和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com