
科目: 来源: 题型:
定量研究是科学研究的重要方法之一,利用它能解决许多生产生活中的实际问题。
(1)将20 g质量分数为4%的氢氧化钠溶液与7.3 g稀盐酸混合,恰好完全反应,所得溶液的pH为7,试计算所用稀盐酸的溶质质量分数。
(2)实验室浓盐酸(分析纯)的溶质质量分数在36%~38%之间为合格药品。(1)题中的稀盐酸是用一定体积(折算成质量为2 g)的浓盐酸(分析纯)加水配制而成的。通过计算判断该浓盐酸是否为合格药品。
查看答案和解析>>
科目: 来源: 题型:
载人宇宙飞船内常用含氢氧化锂(LiOH是一种可溶性碱,具有碱的通性)的过滤网吸收宇航员呼出的CO2,以净化空气。若载人宇宙飞船内每名宇航员平均每天呼出的CO2为550升,请回答:
(1)每天吸收一位宇航员呼出的CO2需氢氧化锂多少克?(列式计算,计算时CO2密度以ρ=2.0 g·L-1计)
(2)载人宇宙飞船使用的过滤网内选用氢氧化锂,而不用价格更便宜的氢氧化钠,其主要原因是___________________________________________________
____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
某实验小组开展了如下有关碱的化学性质探究活动:
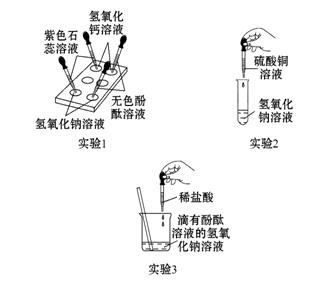
(1)实验1的目的是________________________________________________;
(2)实验2中发生反应的化学方程式是_______________________________;
(3)实验3中观察到溶液由红色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是____________________________
____________________________________;
(4)通过上述实验探究活动,可以总结出碱的化学性质是
①碱能与酸发生中和反应;
②_______________________________________________________________;
……
(5)准备实验时,小英发现药品室有两瓶未标注浓度的氢氧化钠溶液,经询问老师得知,该两瓶溶液的溶质质量分数分别为5%和10%。请你设计实验方案完成对这两瓶溶液的鉴别(仅限以下实验用品:试管、量筒、滴管、酚酞溶液、10%盐酸)。
| 实验步骤 | 预计现象及相应结论 |
| ________________ | ________为5%的氢氧化钠溶液,另一种为10%的氢氧化钠溶液 |
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,请你一起参与。
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】猜想①:氢氧化钙溶液可能全部变质,变为碳酸钙。猜想②:氢氧化钙溶液可能部分变质,其成分是___________________________。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸,充分振荡 | 有______ 生成 | 原溶液中一定含有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液呈红色 | 原溶液中含有______ |
【实验结论】综合上述实验(1)、(2),你得出的结论是猜想________成立。
【反思与拓展】(1)氢氧化钙露置于空气中容易变质,原因是 ___________
__________________________________(用化学方程式表示)。
(2)在分析化学反应前后的物质成分时,除了考虑生成物外,还需考虑的是__
________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下图以稀硫酸为例的反应关系体现了酸的化学性质,其中的X与图中所给物质的类别不同。结合此图回答下列问题:

(1)稀硫酸中阳离子的符号是________;
(2)反应①中石蕊溶液变为________色;
(3)反应②的化学方程式为_____________________________________;
(4)图中只生成盐和水的反应包括_____________________________(填序号);
(5)若X溶液既能跟稀硫酸反应,又能跟Ca(OH)2反应,则X可能是BaCl2、CuSO4、Na2CO3中的________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
二氧化碳的“捕捉”与“封存”是实现温室气体减排的重要途径之一。实际生产中,经常利用足量NaOH溶液来“捕捉”CO2,流程图如下(部分条件及物质未标出)。

(1)分离室中进行的操作是_________________________________________。
(2)该流程图所标出的物质中,溶于水放出大量热的氧化物是________。
(3)“捕捉室”内发生反应的化学方程式为______________________________。
(4)将CaO加入到x溶液中,其中发生复分解反应的化学方程式是__________
__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
从微观的角度认识物质及其变化,更有助于了解物质组成及变化的本质。

(1)图1粒子中,属于阴离子的有________(填序号,下同);在化学反应中最易失去电子的是________________________________________;
由②、③构成的物质的化学式为____________________________________。
(2)图1粒子所属元素可以组成多种化合物,请写出由上述某些元素组成的一种酸的化学式:______________________________________________________,
一种碱的化学式:__________________________________________________。
(3)如图2表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是____________结合生成水,请写出一个与上述反应本质相同的化学反应方程式:________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
盐酸是一种用途广泛的物质,在实验室中用盐酸与其他物质反应可以制得多种气体,其中一种气体的化学式是________。盐酸在工业上有多种用途,其中一种用途是___________________________________________。
四氯化硅(SiCl4)是制造半导体材料硅的中间原料,在空气中容易吸收水蒸气生成H4SiO4和HCl而产生白色烟雾,这一过程的化学方程式是________________
__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
从图像获取信息是化学学习的重要技能。在分析图像时,要注意横坐标与纵坐标表示的含义。结合表格与图进行分析,能够正确的反映图像关系的选项是( )

| 选项 | 变化过程 | 横坐标表示 | 纵坐标表示 |
| A | 氧化钙固体敞口放置在空气中 | 放置时间 | 固体质量 |
| B | 向氢氧化钙溶液中逐滴加入碳酸钠溶液至过量 | 碳酸钠 溶液质量 | 沉淀质量 |
| C | 向20℃的不饱和氯化钠溶液中逐渐加入氯化钠固体 | 加入氯化钠 固体质量 | 溶剂质量 |
| D | 向氢氧化钠溶液中逐渐加水 | 水的质量 | 溶液pH |
查看答案和解析>>
科目: 来源: 题型:
下列关于科学实验的“操作—现象—结论”的描述正确的是( )
A.在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐
B.在某溶液中加入氯化钡溶液和稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子
C.某溶液用pH试纸测试,试纸变蓝色(pH约为10),该溶液一定是碱性溶液
D.在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞试液不变色,可以断定两者恰好完全反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com