
科目: 来源: 题型:
现有常温下0.1 mol·L-1纯碱溶液。
(1)你认为该溶液呈碱性的原因是(用离子方程式表示)_____________________
___________________________________________________;
为证明你的上述观点,请设计一个简单的实验,简述实验过程:
________________________________________________________________________。
(2)同学甲认为该溶液中Na2CO3的水解是微弱的,发生水解的CO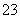 不超过其总量的10%。请你设计实验证明该同学的观点是否正确:
不超过其总量的10%。请你设计实验证明该同学的观点是否正确:
________________________________________________________________________。
(3)同学乙就该溶液中粒子之间的关系写出了下列四个关系式,你认为其中正确的是( )
A.c(Na+)=2c(CO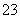 )
)
B.c(CO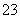 )>c(OH-)>c(HCO
)>c(OH-)>c(HCO )>c(H2CO3)
)>c(H2CO3)
C.c(CO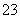 )+c(HCO
)+c(HCO )=0.1 mol·L-1
)=0.1 mol·L-1
D.c(OH-)=c(H+)+c(HCO )+2c(H2CO3)
)+2c(H2CO3)
(4)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),请写出Na2CO3第一步水解反应的水解常数的表示式:__________________________________。
查看答案和解析>>
科目: 来源: 题型:
水的电离平衡曲线如图所示:

(1)若以A点表示25℃时水电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从______增加到________。
(2)将pH=8的氢氧化钡溶液与pH=5的盐酸溶液混合并保持100℃恒温,欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为________。
(3)已知AnBm的离子积K=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)和c(Bn-)表示离子的物质的量浓度。在某温度下,氢氧化钙溶解度为0.74 g,其饱和溶液密度设为1 g/cm3,其离子积为K=________。
查看答案和解析>>
科目: 来源: 题型:
(1)体积相同,浓度均为0.2 mol·L-1的盐酸和CH3COOH溶液,分别加水稀释10倍,溶液的pH分别变成m和n,则m与n的关系为________。
(2)体积相同,浓度均为0.2 mol·L-1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为________。
(3)体积相同,pH均等于1的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为________。
(4)体积相同,pH均等于13的氨水和NaOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成9,则m与n的关系为________。
查看答案和解析>>
科目: 来源: 题型:
现有一份NaOH固体样品,里面混有少量的Na2CO3、NaCl杂质,某同学用中和滴定的方法来测定NaOH的纯度。其操作如下:
①称取a g样品放入锥形瓶中,加水,振荡,使固体充分溶解。
②向该溶液中加入足量的BaCl2溶液,使CO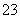 沉淀完全。
沉淀完全。
③向所得混合液中滴入2~3滴酚酞指示剂,然后用c mol·L-1的盐酸进行滴定。
④当反应达终点时,测得消耗盐酸的体积为V mL。
⑤计算样品的纯度。
试回答下面的问题
(1)滴定终点时溶液颜色如何变化:__________________________________________。
(2)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,是否会对NaoH的含量测定造成影响(填“是”或“否”)______,理由是___________________________________。
(3)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,能否改用甲基橙作指示剂(填“是”或“否”)______,理由是________________________________________。
(4)根据上述实验数据,列出计算NaOH纯度的表达式
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中c(HA)________c(A-);
(2)混合溶液中c(HA)+c(A-)________0.1 mol·L-1;
(3)混合溶液中由水电离出的c(OH-)______0.2 mol·L-1 HA溶液中由水电离出的c(H+);
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
查看答案和解析>>
科目: 来源: 题型:
室温时,将x mL pH=a的稀NaOH溶液与y mL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是( )
A.若x=y,且a+b=14,则pH>7
B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7
D.若x=10y,且a+b=14,则pH>7
查看答案和解析>>
科目: 来源: 题型:
向1.0 L 0.30 mol·L-1的NaOH溶液中缓慢通入8.8 g CO2气体,使其完全反应,对反应后的溶液,下列判断正确的是( )
A.溶质为Na2CO3
B.溶质为NaHCO3
C. c(Na+)=c(HCO
c(Na+)=c(HCO )+c(CO
)+c(CO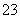 )+c(H2CO3)
)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO )+2c(CO
)+2c(CO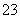 )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
对于重水D2O,在25℃时,KW=10-12,定义pD=-lgc(D+),则下列关于pD说法正确的是( )
A.25 ℃时,纯重水pD=7
B.25 ℃时,0.1 mol·L-1NaCl的重水溶液pD=pOD
C.25 ℃时,1 mol·L-1DCl的重水溶液pD=0,pOD=14
D.25 ℃时,0.1 mol·L-1NaOD的溶液中pD=10
查看答案和解析>>
科目: 来源: 题型:
在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是( )
A.1∶9 B.1∶1 C.1∶2 D.1∶4
查看答案和解析>>
科目: 来源: 题型:
下列关于电解质溶液中离子关系的说法正确的是( )
A.0.1 mol·L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO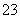 )+c(HCO
)+c(HCO )+c(H2CO3)
)+c(H2CO3)
B.0.1 mol·L-1 NH4Cl和0.1 mol·L-1 NH3·H2O等体积混合后离子浓度关系:c(Cl-)>c(NH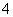 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-)
D.常温下,在pH=1的溶液中,Fe2+、NO 、ClO-、Na+能大量共存
、ClO-、Na+能大量共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com