
科目: 来源: 题型:
小明用如图装置 来测定空气中氧气的含量,对该实验认识正确的是( )。
来测定空气中氧气的含量,对该实验认识正确的是( )。
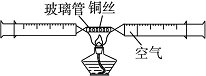
A.使用铜丝的量多或量少,都不会影响实验结果
B.加热足量的铜丝可使注射器内减少的体积占原气体体积的4/5
C.铜丝加热后消耗空气中的氧气,使注射器内压强下降,体积减小
D.实验一停止加热,就要立即观察,并记录剩余气体的体积
查看答案和解析>>
科目: 来源: 题型:
空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应.图1是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程.请按要求回答下列问题:

(1)步骤①中发生的是 变化(填“物理”或“化学”).
(2)写出步骤③中发生反应的化学方程式 .
(3)上述化学反应中属于化合反应的有 个.
(4)图2是化肥硝酸铵包装袋上的部分说明:硝酸铵应具有的性质是 (填字母).
A.易溶于水 B.有挥发性 C.受热易分解
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与熟石灰反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
碳及碳的化合物间的转化关系可表示为: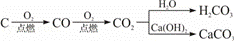 ,由此可写出各步反应的化学方程式.硫及硫的化合物间的转化关系可表示为:
,由此可写出各步反应的化学方程式.硫及硫的化合物间的转化关系可表示为: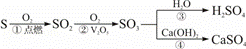 .
.
(1)模仿碳及碳的化合物间转化反应方程式的书写,写出硫及硫的化合物转化反应中指定反应的化学方程式:反应①: ;反应③: .
(2)反应②中,V2O5在反应前后的质量均为m,则V2O5在该反应中起 作用.
(3)上述反应中,属于化合反应的有: (填反应序号).
(4)实验室因操作不当,将浓硫酸滴在书页上,一会书页出现了黑色,且由糊状至烂洞状.这是因为浓硫酸具有 .
查看答案和解析>>
科目: 来源: 题型:
金属钛(Ti)具有熔点高、密度小、抗腐蚀、易于加工等优良性能,被誉为“未来的金属”.工业上以钛酸亚铁(FeTiO3)等原料经过一系列反应制备纳米TiO3和钛,主要生产过程如下:(其他产物已略去)
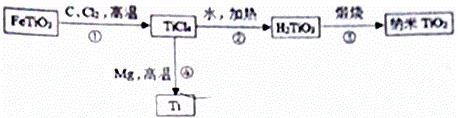
(1)反应①生成两种氯化物和一种有毒的氧化物气体,该气体的化学式是 .
(2)反应②中的化学方程式是 .
(3)纳米TiO2中钛元素和化合价为 价.
(4)反应①②③④中属于置换反应的是 (填序号)
查看答案和解析>>
科目: 来源: 题型:
工业上,通过如下转化可制得KClO3晶体:NaCl溶液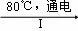 NaClO3溶液
NaClO3溶液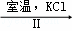 KClO3晶体
KClO3晶体
(1)完成Ⅰ中反应的化学方程式:NaCl+3H2O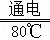 NaClO3+3 ↑
NaClO3+3 ↑
(2)Ⅱ中析出晶体后的母液是KClO3的 (填“饱和”或“不饱和”)溶液,写出母液中的所有溶质的化学式
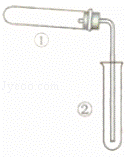
(3)用如图装置(夹持、加热装置已略)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是
| 选项 | ①中实验 | ②中现象 |
| A | 加热氯化钾和二氧化锰的混合物 | 伸入试管内的带火星木条复燃 |
| B | 加热碱式碳酸铜固体 | 澄清石灰水变浑浊 |
| C | 加热铜丝 | 伸入水中导管口有气泡冒出 |
| D | 加热氯化铵和熟石灰的混合物 | 酚酞溶液变红 |
查看答案和解析>>
科目: 来源: 题型:
Na2SO4是制造纸张、药品、染料稀释剂等的重要原料.某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图1所示
(1)加入Na2CO3溶液可除去的阳离子是 (填离子符号),其反应的化学方程式为: .若添加的NaOH溶液和Na2CO3溶液过量,可加入适量 (填名称)除去.
(2)操作a的名称是 ,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、 .
(3)溶液M中的溶质是Na2SO4和杂质NaCl,观察图2中溶解度曲线,则操作b是:先将溶液M蒸发浓缩,再降温结晶、过滤.降温结晶的最佳温度范围是 ℃以下,因为Na2SO4溶解度 .
查看答案和解析>>
科目: 来源: 题型:
氯酸钾多用来制造火柴和烟花等.工业上通过如图1转化可制得氯酸钾晶体.
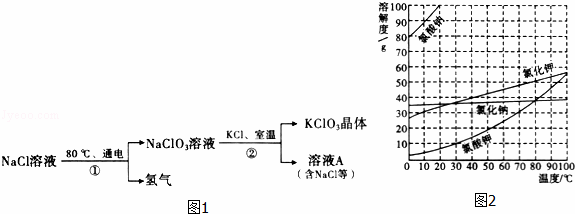
结合图2的溶解度曲线,回答下列问题.
(l)副产品氢气的一种用途: .
(2)80℃的氯化钠溶液中,氣化钠与水的质量为7:20,该溶液是 (填“饱和”或“不饱和”)溶液.
(3)10℃时,图2中四种物质的饱和溶液,其中 溶液的溶质质量分数最小.
(4)配平反应①的化学方程式:□NaCl+□H2O □NaClO3+□H2↑
□NaClO3+□H2↑
(5)反应②的基本反应类型是 ,该反应能发生的原因是 .
(4)生产过程中,溶液A可循环利用,其优点是 (任写一点).
查看答案和解析>>
科目: 来源: 题型:
黄铜矿(主要万分CuFeS2)经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜.主要步骤如图所示:
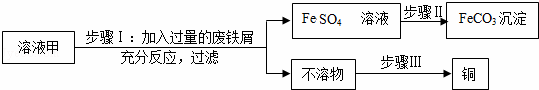
(1)Fe2(SO4)3与铁反应的化学方程式:xFe2(SO4)3+yFe=zFeSO4,其中x、y、z为化学计量数,z的值为 .
(2)步骤Ⅰ中,生成铜的化学方程式: .
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是 .
(4)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是 (填化学式).
(5)步骤Ⅲ回收铜的方法为 .
查看答案和解析>>
科目: 来源: 题型:
现有工厂丢弃的废铜屑(铜屑表面呈绿色,其中混有少量生锈铁屑).课外活动小组同学欲利用其制取胆矾,他们设计了下面的两种制取流程.已知:Cu+Fe2(SO4)3=2FeSO4+CuSO4.请回答:

(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ;操作①所用到的玻璃仪器有:烧杯、玻璃棒和 .
(2)溶液A的溶质有 (只写一种);铁锈与稀硫酸反应的化学方程式为 .
(3)两种方法比较,符合绿色化学要求的是方法 ;方法Ⅱ的化学反应方程式为:2Cu+2H2SO4+ ═2CuSO4+ ;操作②的实验步骤为: 、降温结晶.
查看答案和解析>>
科目: 来源: 题型:
工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:
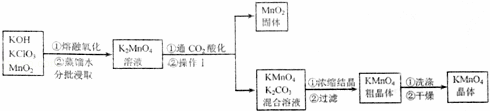
已知相关物质的溶解度(20℃)如下表:
| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
(1)KMnO4中锰元素的化合价为 .
(2)操作Ⅰ的名称是 .“干燥”过程中温度不宜过高的原因是 (用化学方程式表示).
(3)“通C02酸化”,反应的化学方程式为:3K2MnO4+2CO2═2KMnO4+MnO2↓十2K2CO3,
若用稀H2SO4酸化,反应的化学方程式为:
3K2MnO4+2H2SO4=2KMnO4+MnO2↓+2K2S04+2H20
工业上不采用稀H2SO4酸化的原因是 .
(4)电解法也可以实现由向K2MnO4向KMnO4的转化,反应的化学方程式为:
2K2MnO4+2H2O 2KMnO4+2KOH十H2↑
2KMnO4+2KOH十H2↑
与“通C02酸化”相比,其优点是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com