
科目: 来源: 题型:
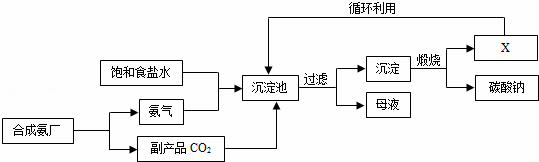
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是()
|
| A. | 沉淀池中的反应物共含有六种元素 |
|
| B. | 过滤得到的“母液”中一定只含有两种溶质 |
|
| C. | 图中X可能是氨气 |
|
| D. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
查看答案和解析>>
科目: 来源: 题型:
某工厂废料中含有铜、氧化铜和碳中的一种或几种。按如下流程进行反应,请回答:

(1)操作Ⅰ的名称是 。
(2)A、C、D、E四种物质中,属于氧化物的是 (填字母)。
(3)蓝色溶液B与锌粉反应的化学方程式是 ,
。
(4)废料的成分是
查看答案和解析>>
科目: 来源: 题型:
黑白复印机用的墨粉中常添加Fe3O4粉末,Fe3O4是由Fe2+、Fe3+和O2﹣按1:2:4的个数比构成的.如图是氧化沉淀法生产复印用Fe3O4粉末的流程简图.已知第④步反应中各元素化合价保持不变.
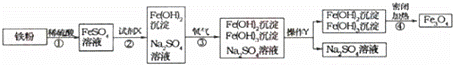
(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是 色.
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为 .
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于 ,才能确保最终生成Fe3O4,操作Y的名称为 .
查看答案和解析>>
科目: 来源: 题型:
南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.
(1)海水制盐.从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发.正确的操作顺序是 (填字母).加Na2CO3溶液的作用是除去 .
(2)海水淡化.如图1是一个简易的蒸馏法淡化海水的装置,证明得到的水是淡水的方法是 .
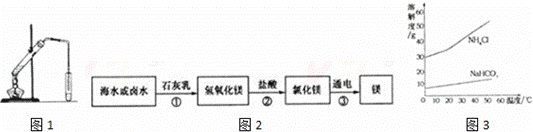
(3)海水制镁.从海水中提取金属镁的过程如图2所示:
在上述转化过程中发生中和反应的是 (填反应顺序号),海水中本身就含有氯化镁,则①、②两步的作用是 .
(4)海水“制碱”.氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱.
①氨碱法制纯碱中生成NaHCO3和NH4Cl的质量比为84:53.5,NaHCO3和NH4Cl的溶解度曲线如图3所示,请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 .
查看答案和解析>>
科目: 来源: 题型:
燃煤产生的烟气中含有二氧化硫,直接排放会污染空气,它与水反应形成酸雨污染环境,某科研小组利用海水除去二氧化硫,其工艺流程见下图:

请回答下列问题:
(1)二氧化硫中硫的化合价是 。
(2)用熟石灰中和稀硫酸的化学方程式是 。
(3)亚硫酸(H2SO3)被空气中氧气氧化为硫酸,写出反应的化学方程式 。
(4)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比——与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g·L-1 | 脱硫率/% |
| I | 23 | 2.5% | 99.5 |
| II | 23 | 3.2% | 97.1 |
| III | 40 | 2.5% | 94.3 |
由表中实验数据可得出的结论是 。
(5)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+。
①反应中Cu+的作用是 。
②除去二氧化硫的总反应的化学方程式是 。
查看答案和解析>>
科目: 来源: 题型:
普通干电池在生活中的用途很广,其构造示意图如右图。回答下列问题:
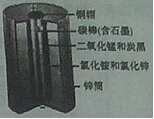
(1)普通干电池胜任照明时化学能转化为 。
(2)电池中石墨表现出优良的 性能;石墨与金刚石物理性质明显差异的原因是 不同。
(3)下图是回收利用废旧普通干电池的一种工艺流程(不考虑废旧电池中实际存在的少量其他物质)。
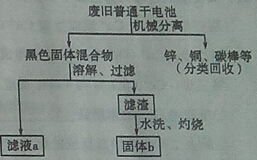
①分离回收铜帽,经净化处理后放入硝酸银溶液中,反应的化学方程式是 。
②滤液a中溶质的化学式是 。
③实验室中在加热和固体b存在的条件下制取氧气,反应的化学方程式是 。
④氯化铵和尿素是重要的化学肥料,请简易鉴别氯化铵和尿素
查看答案和解析>>
科目: 来源: 题型:
探秘海滩上的物质
在海滩上,你能看到各种各样的物质,除海洋生物外,最常见的有海沙,贝壳和海水,虽然他们性质与用途各异,但从元素组成的角度看,这些物质都是由氧、硅、氟、钾、钙等有限的几种元素组成的.
原子是构成物质的“基石”,一种原子,可以构成最常见的单质,但更多的是和其他原子结合成各种化合物,请回答:
(1)从化学的视角认识物质
①海沙是由石英和贝壳的碎片组成,石英的主要成分是(用化学符号表示,下同)贝壳的主要成分是 ;
②请写出一种同时符合下列两个条件的化合物的名称或化学式
(Ⅰ)由氧、硅、氟、钾、钙五种元素中的三种组成;
(Ⅱ)根据分类,与①中两种物质的主要成分类别不同
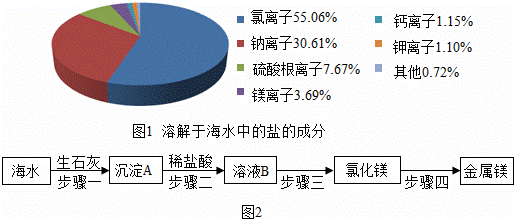
③海水中含有多种无机盐,各离子的含量如图1所示,其中由硫酸根离子和镁离子构成的化学式是 ,假设海水中无机盐的含量为3.8%,钾离子全部以氯化钾的形式存在,则Wg海水中含有氯化钾质量的计算公式为 .
④各地海水中盐的含量并不完全相同,在接近入海口处,海水中盐的含量较低,原因是 .
⑤食用微钠盐可预防高血压,低碘盐是在氯化钠中加了氯化钾,氯化钾除了有咸味外,还带有苦味,从物质构成的角度看,氯化钾有苦味可能是 造成的.
(2)用化学的方法改造物质
海水中含有丰富的镁元素,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图2:
①步骤一中发生反应的化学方程式为 , .
②上述生产流程中发生的反应,没有涉及到的基本反应类型是 置换反应 .
③在步骤一中,分离出沉淀A的方法是 .
查看答案和解析>>
科目: 来源: 题型:
海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧.如图是某厂生产纯碱的工艺流程图:
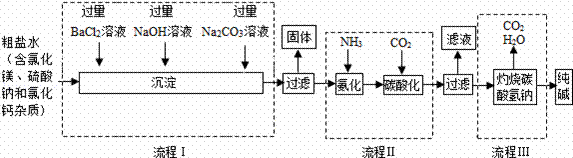
请完成下列问题:
(1)该厂最终产品有 (填物质名称);
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是 (填字母序号);
A.加入三种溶液的顺序不能调整B.加入三种溶液将粗盐水中的SO42﹣、Mg2+、Ca2+转化为沉淀C.按流程I所加溶液的顺序除杂,过滤后得到四中沉淀
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化氨,氨气在制碱过程中的作用是 ;
(4)写出流程Ⅲ中发生反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验.
实验一:(如图1)
(1)写出步骤①中发生的化学方程式 ,此反应的基本类型是 .
(2)步骤②中的操作a名称是 ;步骤③中加入稀盐酸的目的是 .
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.9 4.7
沉淀完全的pH 3.2 6.7
(3)如图2,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整: ,把试纸显示的颜色与标准比色卡比较,读出该溶液的pH.
(5)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理.
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
查看答案和解析>>
科目: 来源: 题型:
控制化学反应的条件可以促进或抑制化学反应,更好使化学反应为人类造福.
(1)如图是科学家正在研究的二氧化碳循环利用技术: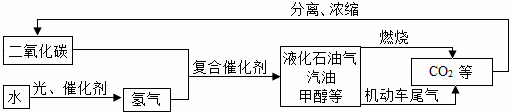
①二氧化碳与氢气在催化剂、高温条件下,除生成甲醇(CH4O)外,还生成一种常温下为液态的化合物,写出反应的化学方程式 ,甲醇中碳元素的化合价为 .
②从图中分析得出的下列结论中,正确的是 AC (填序号)
A.该技术符合低碳经济的理念.
B.水生成氢气的过程中所用的催化剂一定是二氧化锰.
C.该技术有助于缓解全球面临的能源危机.
D.液化石油气、汽油、甲醇均有碳、氢、氧三种元素组成.
(2)汽油燃烧时氧气浓度越大,燃烧越剧烈,试从微观角度解释这是因为 .
(3)尿素[CO(NH2)2]对提高粮食产量具有重要的作用.人们控制条件可以使CO2和物质M发生反应:CO2+2M═CO(NH2)2+H2O,物质M的化学式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com