
科目: 来源: 题型:
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。
(1)海水晒盐的原理是_) ;
 (2)晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图t2℃时,MgCl2的溶解度为_ g.将t2℃时MgCl2、KCl和MgS04三种物质的饱和溶液分别降温至t1℃时,析出的晶体是_ (填物质化学式);
(2)晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图t2℃时,MgCl2的溶解度为_ g.将t2℃时MgCl2、KCl和MgS04三种物质的饱和溶液分别降温至t1℃时,析出的晶体是_ (填物质化学式);
(3)将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加人一定质量的氯化钠并充分溶解。4组实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化納的质量/g | 4.5 | 9 | 18 | 20 |
| 溶液质量/g | 54.5 | 59 | 68 | 68 |
若将②中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是__g;
关于上述实验的叙述不正确的是_ (填字母序号)。
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C. 20℃时,氯化钠的溶解度为36g
D. 20℃时,将④恒温蒸发25g水,过滤得18g固体
查看答案和解析>>
科目: 来源: 题型:
实验室配制500克溶质质量分数为0.5%的高锰酸钾溶液,用于对种子进行消毒。现准备如下实验用品,请回答下列问题:

⑴称量高锰酸钾固体时,药品应放在托盘天平 (填“左”或“右”)盘的纸片上,天平上的游码位置应是下图的 (填字母)。

⑵量取所需水时,除上述准备的实验用品外,还需要的一种仪器是 (填名称)。若仰视读数,则所配制的溶液,其溶质的质量分数会 (填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
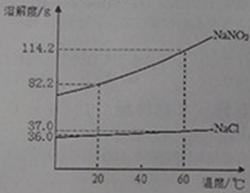
亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似。人若误食会引起中毒,NaNO2、NaCl的溶解度曲线如图所示。
请回答下列问题:
⑴某同学设计的鉴别NaNO2、NaCl固体的方案如下:20℃,取6.0克NaNO2和6.0克NaCl分别放入两只小烧杯中,各加入10mL水(水的密度为1g/mL)。用玻璃棒充分搅拌后,观察现象。你认为此方案是否可行? (填“可行”或“不可行”)。
⑵除去NaNO2固体中混有的少量NaCl,实验步骤:加水溶解、蒸发浓缩、 ,然后过滤、洗涤、干燥。
⑶20℃时,将182.2克NaNO2饱和溶液蒸发掉50克水,再降温到20℃,可析出晶体的质量为 。
⑷分别将60℃时等质量的NaNO2、NaCl的饱和溶液降温到20℃,析出晶体最多的是
(填“NaNO2”或“NaCl”)。
 |
查看答案和解析>>
科目: 来源: 题型:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 |
 |
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如上图),图中能表示碳酸钠溶解度曲线的是 (填“A”或“B”)。
(2)图中两溶解度曲线相交于M点,此点表示的意义是 。
(3)40℃时,把50 g A物质放入100 g水中,充分搅拌,所得溶液是 饱和 溶液(填“饱和”或“不饱和”)。
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”。请你答出“冬天捞碱”的道理 。
查看答案和解析>>
科目: 来源: 题型:
如图是甲、乙两种固体物质的溶解度曲线.据图回答:
(1)10℃时,甲物质的溶解度 乙物质的溶解度.(填“>”或“=”或“<”)
(2)把30℃时等质量的甲、乙两物质饱和溶液降温到10℃,析出晶体较多的是 .
(3)20℃时,将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为 g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶液中不变的是 (填序号).
A.溶剂的质量 B.溶液的质量 C.溶质的质量分数 D.以上都不变.

查看答案和解析>>
科目: 来源: 题型:
水在生活、生产和化学实验中起着十分重要的作用.
(1)水的净化.向浑浊的天然水中加入明矾,静置一段时间后,取上层液体过滤,得到略带颜色的液体.实验中加入明矾的作用是 ,过滤操作中用到的玻璃仪器有烧杯、玻璃棒、 (填仪器名称),其中玻璃棒的作用是 .
(2)水的组成.用如图1实验装置可以证明水的组成,检验a处气体的方法是 .
(3)水的用途.水是常用的溶剂.如图2为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线.
①t1℃,若将4.0g甲物质放入10g水中充分溶解得到 g溶液.
②若固体乙中混有少量固体甲,提纯乙的方法是:溶解、 过滤.
③将t2℃时丙的饱和溶液降温到t1℃时,丙溶液为 (填“饱和”或“不饱和”)溶液,溶质质量分数 (填“变大”、“变小”或“不变”).

查看答案和解析>>
科目: 来源: 题型:
在日常生活和工农业生产中,溶液有着广泛的应用。比如,氨碱工业用到的是饱和食盐水,医疗上使用的则是0.9%的生理盐水。请按要求设计并完成一下实验:实验用品:氯化钠溶液、氯化钠、硝酸钾、蒸馏水、烧杯、试管、玻璃棒、药匙
探究实验一:澄清透明的氯化钠溶液是否是饱和溶液
| 实验步骤 | 实验现象 | 实验结论 |
| 取一只试管倒入约5 mL氯化钠溶液 ,用 药匙加入少量氯化钠固体,振荡,观察现象 | 氯化钠固体溶解 |
探究实验二:将不饱和氯化钠溶液变为饱和溶液并探究饱和氯化钠溶液还能否溶解硝酸钾
| 实验步骤 | 实验现象 | 实验结论 |
| 有固体不再溶解 | NaCl不饱和溶液 变为饱和溶液 | |
| 硝酸钾固体溶解 | 饱和的氯化钠溶 液能溶解硝酸钾 |
查看答案和解析>>
科目: 来源: 题型:
我国海岸线长达3.2万千米,海洋专属经济区幅员辽阔,海洋资源丰富,开发前景十分远大。
(1) 我国海盐年产量3千多万吨,居世界第一位,目前从海水中提取食盐的方法主要为
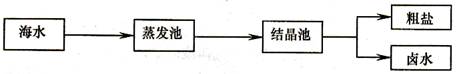
在蒸发池中促进水分蒸发,主要是利用了下列各项中的____(填选项序号)。
①潮汐能 ②生物能 ③电能 ④太阳能 ⑤化学能
(2)金属镁广泛应用于生活、生产和国防工业。从卤水中提取镁的过程如F图所示:

 在上述转化过程中,①处所发生的反应属于__________反应(填“中和”“复分解”“氧化”“化合”“分解”之一)。
在上述转化过程中,①处所发生的反应属于__________反应(填“中和”“复分解”“氧化”“化合”“分解”之一)。
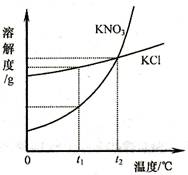
(3)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如右图所示。试回答下列问题:
①t1℃时,KCl饱和溶液的溶质质量分数 KNO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②已知20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g。在20℃时,向盛有200g水的烧杯中加入80℃,在该温度下,最后所得溶液中溶质与溶剂的质量之比为____________________(填最筒整数比)。
查看答案和解析>>
科目: 来源: 题型:
下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 32 | 64 | 110 | 169 | 246 |
⑴从表中数据可以看出NaCl和KNO3的溶解度随温度升高而 (填“增大”或“减小”)
⑵若将KNO3的不饱和溶液变为相同温度下的饱和溶液,其方法为 (填一种)。
若KNO3的饱和溶液中含有少量NaCl时,提纯的方法是 (填一种)。
⑶下列有关说法正确的是
a.40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大
b.KNO3饱和溶液中一定不能再溶解NaCl固体
C.从表中数据可以判断NaCl和KNO3的溶解度相等的温度在20~40℃之间
查看答案和解析>>
科目: 来源: 题型:
如图是甲、乙两种固体物质的溶解度曲线.据图回答:
(1)P点的含义 .
(2)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有 (写出一种),当甲中含有少量乙时,可采用 的方法提纯甲.
(3)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为 .若烧杯内物质升温到50℃(不考虑蒸发 ),溶液中变化的是 (选填序号).
a.溶质的质量 b.溶液的质量 c.溶质的质量分数
(4)从图中还可获得的信息是 (答出一条).
 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com