
科目: 来源: 题型:
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.
(1)C的元素符号是 ;元素F在周期表中的位置 .
(2)B、D、E元素的氢化物的沸点高低顺序为 > > (用化学式表示).
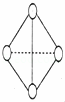
(3)C4气态分子结构如图所示,已知断裂1molC﹣C吸收l67KJ的热量,生成lmol C≡C放出942KJ热量.试写出由C4气态分子变成C2气态分子的热化学方程式 .
(4)某盐x (C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.
①盐x显酸性原因(用离子方程式表示) .
②写出足量金属镁加入盐x的溶液中所发生反应的化学方程式
.
(5)E所在周期中原子半径最大的元素与D元素可形成化合物у,酚酞试液遇у先变红后褪色,写出等物质的量的у与FeSO4投入水中恰好完全反应的离子反应方程式 .
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z、W、Q都是周期表中短周期的元素,它们的核电荷数依次增大.其中X、Y、Z是同周期的非金属元素.W的三价阳离子与Z的阴离子具有相同的电子层结构,它们相互形成的化合物中存在离子键;XZ2为非极性分子;Y、Z 氢化物的沸点比它们同族其他元素氢化物的沸点高;Q在同周期元素中原子半径最小.
回答下列问题:
(1)写出化合物XZ2的电子式 ,其晶体类型为 .
(2)Y、Z 氢化物的沸点比它们同族元素氢化物的沸点高的原因是 .
(3)将少量YZ2通入过量小苏打溶液中,再使逸出的气体通过装有足量过氧化钠颗粒的干燥管,最后收集到的气体是 .
(4)某温度下,在2L密闭容器中投入0.2mol H2和0.2mol XZ2,发生如下反应:H2+XZ2⇌H2Z+XZ 测得平衡时,XZ2的转化率为60%,则该温度下的平衡常数为 .
(5)高铁酸钾(K2FeO4)是一种新型的高效氧化剂和消毒剂,常用于饮用水处理.工业生产高铁酸钾的方法为:①常温下先将Q的单质通入氢氧化钠溶液中制得含Q元素的一种含氧酸盐;②再将其与氢氧化钠溶液混合氧化硝酸铁,得到高铁酸钠粗产品;③过滤后用氢氧化钾溶液溶解,重结晶,再经过脱碱、洗涤、干燥处理,得到高铁酸钾.写出②中发生反应的离子方程式 ,第③步中高铁酸钠能够转化为高铁酸钾的原因是 .
查看答案和解析>>
科目: 来源: 题型:
常温常压时,下列叙述不正确的是( )
A.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa)
B.pH=5的①NH4Cl溶液②CH3COOH溶液③稀盐酸溶液中c(H+)水:①>②>③
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.0.1 mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则b<a+l
查看答案和解析>>
科目: 来源: 题型:
关于下列四个图象的说法中正确的是( ) 
A.图①t1时改变的条件可能是升高了温度或增大了压强
B.图②该微粒仅为18O2﹣不能为16O2﹣
C.图③若A为CaO,则B可能为MgO
D.图④中的△H1<△H2
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.HIO与HCN均为含有极性键的直线形极性分子
B.SiO2与C02均为每摩含有4×6.02×1023对共用电子对的酸性氧化物
C.Na2S浓溶液与稀盐酸分别滴加到饱和AgCl溶液中均一定有沉淀产生
D.明矾与离子交换树脂均能将海水进行淡化
查看答案和解析>>
科目: 来源: 题型:
对图装置说法正确的是( )
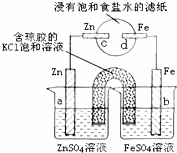
A.a电极上发生还原反应
B.盐桥中的阴离子向b电极移动
C.一段时间后,c电极区溶液的pH降低
D.一定时间内,向d电极区滴入黄色K3[Fe(CN)6]溶液,可能出现Fe3[Fe(CN)6] 2蓝色沉淀
查看答案和解析>>
科目: 来源: 题型:
下列实验装置设计正确、且能达到目的是( ) 
A.实验Ⅰ:静置一段时间,小试管内有晶体析出
B.实验Ⅱ:制取O2
C.实验Ⅲ:除CO2气体中的HCl
D.实验Ⅳ:配制一定物质的量浓度的稀硫酸
查看答案和解析>>
科目: 来源: 题型:
下列溶液中离子一定能够大量共存的是( )
A.加入Al能放出H2的溶液中:Cl﹣、SO42﹣、NO3﹣、Mg2+
B.能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42﹣、S2﹣、SO32﹣
C.c(H+):c(OH﹣)=1:1012的水溶液中:CO32﹣、Na+、NO3﹣、AlO2﹣
D.无色溶液中:K+、Na+、MnO4﹣、SO42﹣
查看答案和解析>>
科目: 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验Cl2管道是否泄漏
B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
C.碳酸氢钠热稳定性弱,用作焙制糕点的发酵粉
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目: 来源: 题型:
 右图是某硝酸铵产品包装袋上的标签说明。仔细分析标签说明,然后回答下列有关问题。
右图是某硝酸铵产品包装袋上的标签说明。仔细分析标签说明,然后回答下列有关问题。
(1)硝酸铵由 ▲ 种元素组成。
(2)硝酸铵的相对分子质量是 ▲ 。
(3)硝酸铵中N、H、O的质量比是 ▲ 。
(4)该硝酸铵产品中所含硝酸铵的质量分数是 ▲ 。
(5)某农民有10亩地,开始准备每亩地需施用66kg纯硫酸铵[(NH4)2SO4]来促进农作物生长,现因纯硫酸铵缺货,改施用上述硝酸铵产品,若要使两种化肥达到相同的肥效(即氮元素的质量相同),则该农民总共需购买多少kg上述硝酸铵产品?(写出计算过程)(2分)
▲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com