
科目: 来源: 题型:
我校初二学生去桐庐瑶琳仙境春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的稀盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得如表数据,试回答:
甲同学 乙同学 丙同学 丁同学
石灰石样品的质量(g) 10.0 10.0 10.0 10.0
加入稀盐酸的质量(g) 20.0 30.0 45.0 50.0
剩余固体的质量(g) 6.0 4.0 1.0 1.0
(1) 同学的实验中稀盐酸有剩余, 同学的实验中碳酸钙有剩余.
(2)样品中碳酸钙的质量分数是,同学们使用的稀盐酸的溶质质量分数是 .
查看答案和解析>>
科目: 来源: 题型:
小科同学想测定Cu﹣Zn合金和Cu﹣Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器.
(1)你认为能测出Cu的质量分数的是 合金;
(2)小科同学取该合金32.5g,与足量的该盐酸充分反应,经测定,产生了0.4g气体.请计算该合金中Cu的质量分数.
(3)若想测出该盐酸的质量分数,你认为实验时必须提供和测出哪些数据? ;
①参加反应的合金质量 ②参加反应的稀盐酸的质量 ③产生气体的质量.
查看答案和解析>>
科目: 来源: 题型:
2015年5月,某市自来水有股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚.将30g邻叔丁基苯酚完全燃烧,生成88gCO2和25.2gH2O(无其他产物).已知邻叔丁基苯酚的相对分子质量为150,求:
(1)CO2中碳、氧元素的质量比 .
(2)30g邻叔丁基苯酚中含碳元素质量是 g.
(2)邻叔丁基苯酚的化学式为 .
查看答案和解析>>
科目: 来源: 题型:
我国早在西汉时期,就能利用铁与硫酸铜溶液反应制取铜,沈括在其《梦溪笔谈》以“曾青得铁化为铜”记之,该反应的化学方程式为 .小张同学对此很感兴趣,他利用硫酸铜进行趣味实验,将浸泡了蓝色硫酸铜溶液的滤纸在酒精灯火焰上点燃,观察到滤纸颜色变白,由湿变干后燃烧.在燃烧后的灰烬中出现红色固体.他很好奇,进行了相关探究.
【提出问题】红色固体是什么物质?它是如何产生的?
【查阅资料】
(1)温度达200℃时,CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变.
(2)温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O),Cu2O呈红色.
【作出猜想】红色固体①可能是Cu;②也可能是Cu2O;③还可能是 .
【实验探究】
(1)取红色固体观赏,呈亮红色;
(2)取少量红色固体于试管中,加入稀硫酸,固体不溶解,溶液仍为无色.
【分析推理】
(1)请教老师后得知,如有Cu2O存在,加入稀硫酸会发生如下反应:Cu2O+H2SO4═CuSO4+Cu+H2O,同学们结合实验探究的现象,确定亮红色固体为 .
(2)滤纸主要是由碳、氢、氧三种元素组成的,经分析,产生红色固体的原因可能是滤纸在燃烧过程中产生的碳与分解产生的CuO发生反应,生成亮红色固体和二氧化碳,该反应的化学方程式 ,这说明滤纸燃烧时的温度低于 ℃.
【交流讨论】
(1)将浸有硫酸铜溶液的滤纸点燃,刚开始不能燃烧,是因为 .
(2)此实验中,CuSO4受热分解生成CuO和 (填化学式).
查看答案和解析>>
科目: 来源: 题型:
化学小组同学对酸的性质很感兴趣,向老师提出研究硝酸的性质,老师高兴答应并带领同学们进行了硝酸性质的实验探究.
【实验设计】
(1)将石蕊试液滴入稀硝酸中,预计石蕊试液由紫色变 色.
(2)将Zn片投入稀硝酸中,预计将产生氢气.
【实验验证】同学们按上述设计做了实验,却发现石蕊变色后一会儿即褪去,Zn片投入稀HNO3后,溶液中冒出气泡,产生无色气体A,在试管口气体A变成红棕色有刺激性气味的气体B.
【提出问题】
(1)石蕊试液变色后为何会褪色?
(2)上述产生的无色气体是什么?硝酸具有哪些特性?
【查阅资料】看到如此异常的现象,在老师的指导下,同学们上网查到了下列资料:
(1)硝酸可与Zn、Cu等多种金属反应生成相应的硝酸盐,但不生成H2.
(2)含有氮元素的某些气态物质的物理性质
NH3 N2 NO NO2
顏色 无色 无色 无色 红棕色
溶解性 极易溶于水 不溶于水 不溶于水 可溶于水或硝酸
【猜想与分析】
(1)小明同学认为石蕊变色后又褪色的原因是由于试管不干净,含有其他杂质造成的,要证明小明的观点,应进行的操作是 .
(2)大家一致认同了红棕色气体B是NO2,但对于无色气体A及变化的原因有不同的看法:
①小丽同学认为A是NH3,但遭到大家的一致反对,原因是 ;
②小强同学认为A是N2,也遭到大家的一致反对,原因是 2 ;
③经讨论,最终大家获得了“A是NO”的共识.NO遇氧变成NO2的化学方程式为 .
【实验探究】小红同学对硝酸能与Cu反应很感兴趣,便取了一小块铜片投入稀HNO3中,发现Cu溶解,也出现上述Zn与稀HNO3反应的类似现象,确证生成了NO,并在老师的帮助下,测出恰好反应的Cu和HNO3的质量比为8:21,由此获得了Cu与稀HNO3的反应方程式为 .
【交流反思】根据探究结果可知,稀HNO3能跟铜反应的原因是硝酸具有氧化性.
查看答案和解析>>
科目: 来源: 题型:
天然气作为燃料已进入千家万户,小聪在帮父母烧菜时想到,天然气燃烧的产物是什么呢?带着这一问题,小聪和同学们一起进行了探究.
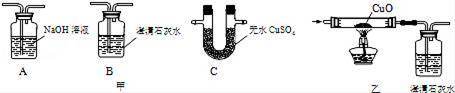

探究一:天然气的主要成分是甲烷(CH4),燃烧后的产物中可能有二氧化碳、水,同学们想利用甲图中的装置进行验证,请你帮助他们选择合理的装置并连接;燃烧后的混合气体应依次通过 装置.
探究二:甲烷燃烧会不会因氧气不足而生成一氧化碳呢?
同学们提出可用乙图装置加以校验,那么气体通入该装置之前应怎样处理?他们讨论后一致认为:先把燃烧后的混合气体依次通过甲图中的A、B、C装置,然后再通入乙图装置.如果看到 现象则表明燃烧产物中有一氧化碳.注意事项:混合气体通过乙装置进行实验时,应先通气体、再加热,这样做的目的是 .小聪认为上述方案还存在缺陷,请你指出来: .
查看答案和解析>>
科目: 来源: 题型:
日常生活中,切开的苹果很快就会
“生锈”.小亮查到了相关资料:当苹果被切开时,
进入的氧气就会与苹果中的一些物质发生反应,使之变成褐色.苹果“生锈”以后,所含的维生素C会减少,影响营养价值.小亮对此展开探究:
猜想:苹果“生锈”可能与空气中的氧气有关.“生锈”的快慢还可能与温度有关.
实验:
实验操作(观察30分钟) 实验结果
甲 将一小块苹果浸入装满蒸馏水(已除去氧气)的集气瓶中,观察现象. 果肉表面不变色
乙 将一小块苹果放入充满氧气的集气瓶中,观察现象. 果肉表面
丙 将一小块苹果放入充满氧气的集气瓶中,再浸入热水里,观察现象. 果肉表面很快变色,颜色很深
(1)由 两组实验可以验证苹果“生锈”是否与空气中的氧气有关;
(2)实验结论之一:苹果“生锈”的速度与温度有关,温度越高,变色越快.请你补充乙组的实验结果:果肉表面 ;
(3)为了防止切开后的苹果“生锈”,可以采取的措施有 .
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组,设计了如图所示装置来研究空气中氮气的体积分数,用一个50mL量筒倒扣在水中,使量筒内内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
(1)加入浓硫酸的目的是 ;
(2)放白磷的小船用铜做的原因是 ;
(3)最终,液面大约位于量筒刻度 处;
(4)为何要向水槽内加水至内外液面相平? ;
(5)该兴趣小组选用的仪器有何缺陷 .


查看答案和解析>>
科目: 来源: 题型:
在A、B、C、D四支试管中分别盛有CuSO4、NaCl、BaCl2、BaCO3四种白色固体,某同学在只有蒸馏水和若干试管的条件下,将它们一一鉴别出来.
(1)步骤一:取四种固体各少量,分别放入4支试管中,各加入适量的水,双察.根据物质的溶解性及溶液的颜色可鉴别出 ;
(2)步骤二:签别余下物质.具体操作方法及相关现象、结论为:有关反应的化学方程式分别为 .
查看答案和解析>>
科目: 来源: 题型:
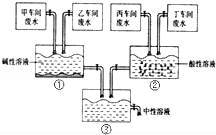
“五水共治”的首要任务是“治废水”,合理处理废水是当前防治废废水染的重要举措.某化工厂有甲、乙、丙、丁四个车间,排放的废水中分别含有FeCl3、HCl、Na2CO3、NaOH的一种.甲车间的废水呈黄色.通过调节废水流量,使乙、丁两个车间废水相对过量,通过如图方式处理,最终可使排出的废水呈中性.处理时第①反应池中出现大量的红褐色沉淀,第②反应池中出现大量的气泡.请回答:
(1)乙车间排放的废水主要成分是 .
(2)写出第②反应池的废水中的溶质有 .(用化学式表示)
(3)写出第③反应池中发生的化学反应方程式: .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com