
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
某化学兴趣小组用青霉素的药瓶、注射器和眼药水瓶设计了如图所示的实验装置,用于检验二氧化碳的性质。缓缓推动注射器活塞,滴入稀硫酸后,在眼药水瓶中即可产生二氧化碳气体,下列有关说法错误的是

A. 该实验中不能用浓盐酸代替稀硫酸
B. 上下两片滤纸条变红,只能证明CO2与水反应生成碳酸
C. 该实验能验证二氧化碳不能燃烧,也不支持燃烧
D. 该微型实验具有所用药品量少,现象明显,操作简单等优点
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
下列归纳和总结完全正确的一组是
A.对物质的认识 | B.对能源的认识 |
①氯化钠由离子构成 ②金刚石和石墨物理性质差异很大,是因为组成元素不同 ③不同的酸具有相似的化学性质是由于酸溶液中含H+ | ①煤、石油、天然气都属于不可再生能源 ②当燃气灶的火焰呈现黄色,锅底出现黑色时,需要调大灶具的进风口 ③开发利用新能源有助于减缓温室效应 |
C.对现象的认识 | D.对健康的认识 |
①花香四溢,说明分子在不断运动 ②打开浓盐酸的试剂瓶盖,有白烟产生 ③电解水生成氢气和氧气的体积比为2: 1 | ①用大量工业用盐亚硝酸钠腌制鱼肉 ②利用甲醛水溶液浸泡水产品防腐 ③适量补充维生素A防止夜盲症 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
盐场晒盐后所得的卤水中含有MgCl2,KCl和MgSO4等物质,它们的溶解度曲线如图所示,下列说法正确的是

A. t1℃时,KCl和MgSO4两溶液所含溶质质量一定相等
B. t2℃时,MgSO4的饱和溶液升高温度和降低温度都能析出晶体
C. t3℃时,100gMgCl2的饱和溶液中含有agMgCl2
D. 将t1℃时的KCl饱和溶液升温到t3℃,溶液的溶质质量分数变大
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
中考复习阶段,小刚同学梳理了以下知识:①NH4NO3属于复合肥料,溶于水溶液温度降低;②利用铁、银、Cu(NO3)2溶液能探究出铜、铁、银的金属活动性顺序;③用湿润的pH试纸来测定稀盐酸的酸碱度;④洗涤剂去除油污是因为洗涤剂具有乳化作用;⑤催化剂只能加快反应速率; ⑥稀有气体原子的最外层电子数都为8;其中正确的是
A. ②④ B. ④⑥ C. ①②④ D. ②③⑤
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
下列实验方案,实验设计达不到实验目的的是
方案 | 实验目的 | 实验设计 |
A | 证明蜡烛燃烧有水生成 | 在火焰上方罩一只干冷的小烧杯 |
B | 鉴别CO和CO2 | 分别通过灼热的CuO |
C | 验证燃烧的条件之一:温度要达到可燃物的着火点 | 将乒乓球碎片和滤纸片置于薄铜片上,用酒精灯火焰加热铜片 |
D | 除去CaCl2溶液中的少量盐酸 | 加入过量的Ca(OH)2溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:选择填充题
一包固体粉末可能含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种。为探究该固体粉末的组成,某化学兴趣小组进行了如下图所示实验:

下列选项错误的是:
A. 原固体粉末中一定不含有NaOH
B. 原固体粉末中一定含有Mg、CuO、KCl,可能含有碳粉
C. 滤液C中一定含有HCl、MgCl2和CuCl2
D. 若检验滤液B中是否有硝酸银剩余,可以将滤液C与滤液B混合,观察实验现象
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:信息分析题
化学就在我们身边,请用所学的化学知识填空。
(1)用适当的化学符号填空
①人体中含量最多的元素是________; ②食醋中含有的酸是_______________;
③极易与血红蛋白结合的有毒气体是____; ④硫酸亚铁溶液中的金属离子是_____。
(2)下图是某同学“自制汽水”的课外实验,请回答下列问题:

①柠檬酸的pH____7(填“<”、“=”或“>”);
②装汽水的塑料瓶属于_________(填“金属材料”或“合成材料”);
③白糖属于人体六大营养素中的______(填“糖类”“油脂”“蛋白质”);
④有关小苏打说法不正确的是____________;
A.属于酸 B.可做焙制糕点的发酵粉
C.能与柠檬酸反应产生二氧化碳 D.可用于治疗胃酸过多症
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:探究题
根据下列装置回答问题。
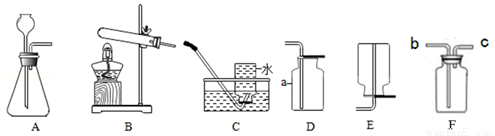
(1)请写出仪器的名称:a_____________。
(2)用高锰酸钾为原料制取较纯净的氧气可选用的装置组合为______(填字母,下同),发生装置应作的改进是_________,发生的化学方程式为________________。
(3)实验室用锌粒和稀硫酸制取氢气,发生的化学方程式为_____________,可选用的发生装置是______,若用F装置收集氢气,气体应从_____端通入(填“b”或“C”)。
(4)某化学兴趣小组设计实验甲、乙(装置如下图)探究二氧化氮气体能否使带火星木条复燃。

【资料】Ⅰ.硝酸铜加热分解生成氧化铜、红棕色二氧化氮气体(有毒)和氧气。
Ⅱ.同温同压下,不同气体的体积之比等于分子个数之比。
①甲实验中硝酸铜加热分解的化学方程式为_______________________,NaOH溶液的作用是____________。
②根据实验过程中的____________________现象得出“NO2能使带火星木条复燃”的结论。请你从气体的组成角度分析,该结论正确的理由是_______________。
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:简答题
p型透明导电化合物CuAlO2具有良好的热电性能,在热电转换领域具有广阔的应用前景。银铜合金广泛用于航空工业,以下为从航空切割废料中回收银并制备CuAlO2的工艺流程。

【资料】
Ⅰ.难溶性碱受热易分解为两种氧化物,Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃;
Ⅱ.CuAlO2高温易分解、受热易氧化。银在空气中不易被氧化。
请回答下列问题:
(1)CuAlO2中铜元素的化合价为______,过滤后所得滤液A中的溶质为__________。
(2)煮沸过程中发生反应的化学方程式为_____________________。
(3)固体B在煅烧时发生的其中一个反应方程式为4CuO + 2Al2O3  4CuAlO2+X↑,气体X的化学式为__________。
4CuAlO2+X↑,气体X的化学式为__________。
(4) “煅烧”时温度须控制在1042—1085℃范围内且在氩气中进行,其原因是________。
查看答案和解析>>
科目: 来源:2017届江苏省无锡市惠山区九年级4月中考模拟化学试卷(解析版) 题型:简答题
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一.高纯CaO的制备
【资料一】
Ⅰ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。

实验过程中发现:B中无水硫酸铜变蓝,C中产生_____________现象证明有SO2生成,装置_____中无明显变化和装置F中_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
二.硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:
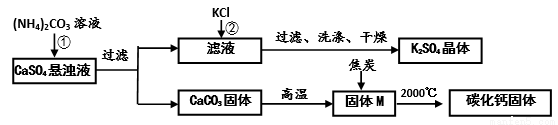
【资料二】氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
(1)反应①的化学方程式为__________________________。证明固体M中不含CaCO3的方法是____________________________(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4 + 2KCl ═ K2SO4↓+ 2NH4Cl,该反应能析出K2SO4晶体的原因是_____________________________________。
(3)假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】碳化钙在空气中灼烧生成氧化钙和二氧化碳气体。
步骤一:称取3.76g样品于下图所示石英管中(测定装置图如下,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)

步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
①装置甲的作用是_______。反应完全后继续缓缓通入空气的目的是_________。
②根据步骤一、二计算该样品中钙、碳、氧的质量比为______________,计算确定CaCx的化学式(请写出计算过程)________。
③应用:丙同学经查阅资料知道实验室常用电石(主要成分为碳化钙)与水反应制取乙炔气体(发生装置如图)。经实验发现,电石与水反应非常剧烈,为控制反应的速度以得到平稳的气流,下列改进方法可行的是______。
A.改长颈漏斗为分液漏斗或注射器 B.将电石研成粉末
C.将锥形瓶置于冰水浴中 D.用饱和食盐水代替水(电石与氯化钠不反应)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com