
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
| 内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | 有白色沉淀,溶液由红色变为无色 | 小兰的猜想正确. |
| 有白色沉淀,溶液呈红色 | 小亮的猜想正确. |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 烧杯、玻璃棒、蒸发皿 硫酸铜溶液的浓缩结晶 | |
| B. | 烧杯、玻璃棒、胶头滴管、滤纸 用水除去二氧化锰中的氯化钾 | |
| C. | 烧杯、玻璃棒、胶头滴管、量筒 用固体碳酸钠配制5%的溶液 | |
| D. | 烧杯、玻璃棒、pH试纸、标准比色卡、玻璃片 测定雨水的酸度 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 试剂1 | 试剂2 | 混合前温度/℃ | 混合后温度/℃ | |
| 30毫升稀盐酸 | 30毫升NaOH溶液 | 20.O | 第1次 | 25.2 |
| 第2次 | 25.O | |||
| 第3次 | 25.4 | |||
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣.
某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣.查看答案和解析>>
科目: 来源: 题型:填空题
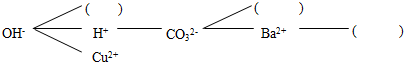
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com