
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
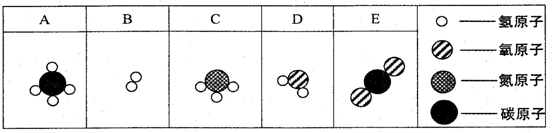
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 锥形瓶+10.0g钙片+50.0g稀盐酸 | 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 199.2 | 198.0 | 197.5 | 196.9 | 196.7 | 196.7 |
查看答案和解析>>
科目: 来源: 题型:解答题
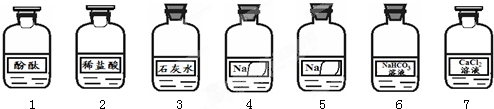
| 实验操作 | 实验现象 | 实验结论 |
| 实验1 滴加适量1号溶液.  | 溶液均由无色变成红色 | 4、5号溶液均不可能是上述猜想中的NaCl溶液. |
| 实验2 滴加适量3号溶液  | 均产生白色沉淀 | 4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
| 实验操作 | 实验现象 | 实验结论 |
滴加适量2号溶液 | 均有气泡产生,5号溶液产生有刺激性气味的气体. | 4号溶液是Na2CO3溶液 5号溶液是Na2SO3溶液. |
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量4号溶液于试管中,加入足量7号溶液. ②向上层清液中滴加无色酚酞溶液. | 有白色沉淀生成,溶液由无色变成红色 | 4号溶液是部分变质的NaOH溶液. |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 盐酸溶 液浓度 | 反应开始时 酸溶液的温度 | 反应开始到2分钟 产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20°C | 10ml | 60ml |
| 10% | 20°C | 19ml | 118ml |
| 15% | 20°C | 28ml | 175ml |
| 5% | 35°C | 28ml | 60ml |
| 10% | 35°C | 72ml | 118ml |
| 15% | 35°C | 103ml | 175ml |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图是浓盐酸试剂瓶上标签的内容.请回答:
如图是浓盐酸试剂瓶上标签的内容.请回答:查看答案和解析>>
科目: 来源: 题型:解答题
 小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.
小明发现二氧化锰催化 过氧化氢分解的实验中,反应速度逐渐变慢.查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低.为了探究二氧化锰催化能力降低的影响因素,进行如下实验.| 组别 | 未使用过的二氧化锰 | A | B | C | D |
| 收集氧气时间/秒 | 17.9 | 23.2 | 27.7 | 32.3 | 37.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com