
科目: 来源: 题型:解答题
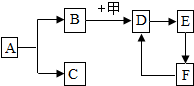 如图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题:
如图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | M中含有氧元素,因此属于氧化物 | B. | M的相对分子质量是42 | ||
| C. | M中氮氧原子个数比为2:1 | D. | 化学正在加快发展 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe→Fe(OH)3 | B. | CaCO3→CaO | C. | CaO→Ca(OH)2 | D. | Na2CO3→NaOH |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
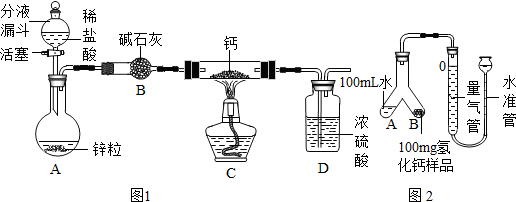
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定有N2和CO,肯定无HCl | B. | 一定有N2和CO,可能有HCl | ||
| C. | 一定有N2、HCl和CO | D. | 一定有CO,可能有N2和HCl |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com