
科目: 来源: 题型:多选题
| A. | 化学面对现代日益严重的环境问题显得无能为力 | |
| B. | 化学将在能源、资源的合理开发和安全应用方面大显身手 | |
| C. | 化学是一门具有极强实用性的科学 | |
| D. | 化学是一门以实验为基础的自然科学 |
查看答案和解析>>
科目: 来源: 题型:解答题
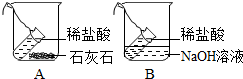 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ④③①②⑤ | B. | ②①④③⑤ | C. | ②④①③⑤ | D. | ④①②③⑤ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在溶洞中,当溶有Ca(HCO3)2的水液发生分解,析出固体(在洞顶或洞底),日久天长便形成了钟乳石 | |
| B. | 长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气压小于瓶外大气压的缘故 | |
| C. | “通风橱”是利用排风扇将橱内废气直接排放到室外的装置,它是种非常完善的防污设施 | |
| D. | 高压氧舱可治疗煤气中毒,原因是和血红蛋白结合的CO跟氧气反应生成无毒的CO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | AG的值越大,溶液的pH越小 | B. | 若某溶液的AG=0,则该溶液的pH=0 | ||
| C. | 25℃时,纯水的AG=0,pH=7 | D. | 25℃时,pH>7的溶液中AG<0 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
查看答案和解析>>
科目: 来源: 题型:解答题
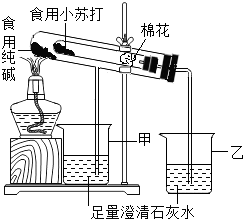 某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com