
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
 如图为A、B两种固体物质的溶解度曲线.
如图为A、B两种固体物质的溶解度曲线.查看答案和解析>>
科目: 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 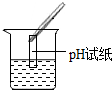 |  |  |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A | 化学变化中的能量变化 | B | 化肥知识 |
| 蜡烛燃烧--放热反应 碳还原二氧化碳--吸热反应 | 钾肥作用--增强抗寒、抗旱能力 使用事项--不能与碱性物质共用 | ||
| C | 元素与人体健康 | D | 化学原理解释生活常识 |
| 缺锌--易引起食欲不振,发育不良 缺钙--易骨质疏松或得佝偻病 | 用氢氧化钠去油污--与油脂反应 用 汽油除去油污--溶解作用 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有①CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量②气泡产生,得到浅绿色溶液. | 固体中一定含有③Fe, 一定不含Fe2O3 |
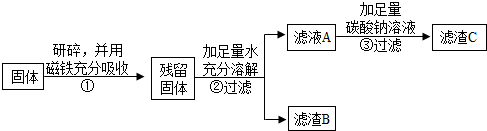
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色溶液变为黄色、澄清的石灰水变浑浊 澄清的石灰水变浑浊 | 固体中一定含有 ③CaCO3和Fe2O3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com