
科目: 来源: 题型:解答题

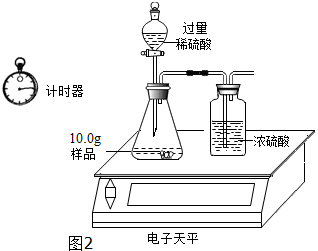
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ①②③ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 大于9mL | B. | 小于9mL | C. | 9mL | D. | 无法判断 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分子由原子构成,所以分子比原子大 | |
| B. | 原子中的原子核一定含有中子 | |
| C. | 原子的最外层电子数跟该原子对应的元素的化学性质关系密切 | |
| D. | 中子和质子是最小的粒子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 禁止焚烧农作物秸秆和垃圾 | B. | 大力植树造林 | ||
| C. | 大力发展煤炭发电 | D. | 用清洁能源代替化石燃料 |
查看答案和解析>>
科目: 来源: 题型:解答题
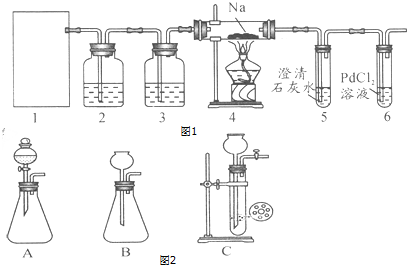
查看答案和解析>>
科目: 来源: 题型:解答题
| 组别 | 药 品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 粉末状石灰石和稀盐酸 | 产生气泡速率很快 |
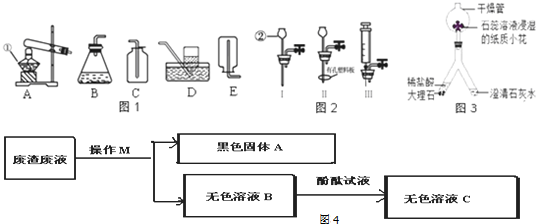
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com