
科目: 来源: 题型:实验探究题
| 编号 | 甲 | 乙 | 丙 | 丁 |
| 所取固体样品质量/g | 5 | 10 | 15 | 20 |
| 所加CaCl2溶液质量/g | 100 | 100 | 100 | 100 |
| 反应后生成沉淀的质量/g | 4 | 8 | 10 | A |
查看答案和解析>>
科目: 来源: 题型:填空题
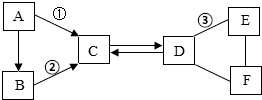 A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)
A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:解答题
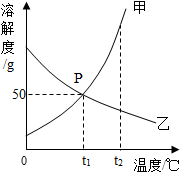 甲、乙两种物质的溶解度曲线如图所示.请回答以下问题:
甲、乙两种物质的溶解度曲线如图所示.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
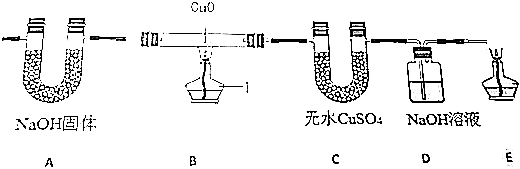
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡直至完全溶解. | 不产生气泡 | 猜想一不成立. |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液. | 产生白色沉淀 | 证明有碳酸钠存在. |
| ③取少量②的溶液于试管中,滴加酚酞试液. | 溶液变红 | 证明有NaOH存在. |
| 综合以上实验现象,说明猜想Ⅱ是成立的. | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com