
科目: 来源: 题型:选择题
| A. | 该化学方程式中m=2 | B. | 该反应中只涉及一种氧化物 | ||
| C. | 该反应属于化合反应 | D. | 该反应中原子的种类发生了变化 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ①滤液不变色 ②有气泡产生 | 氢氧化钙全部 变为碳酸钙 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ① ② |
查看答案和解析>>
科目: 来源: 题型:填空题
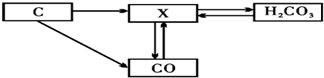
查看答案和解析>>
科目: 来源: 题型:填空题
 金属材料在生产和生活中应用十分广泛
金属材料在生产和生活中应用十分广泛查看答案和解析>>
科目: 来源: 题型:解答题
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.查看答案和解析>>
科目: 来源: 题型:解答题
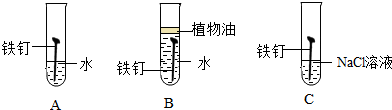

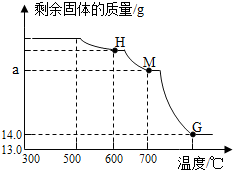
查看答案和解析>>
科目: 来源: 题型:解答题
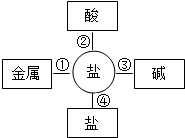 (1)请选择K、H、N、O、C中恰当的元素填写下列物质的化学式:
(1)请选择K、H、N、O、C中恰当的元素填写下列物质的化学式:| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 | 污渍爆炸盐 |
| 产品样式 |  |  |  |  |  |
| 有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过氧化氢 | 过碳酸钠 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤⑦ | B. | ②③④⑦ | C. | ①②⑥⑦ | D. | ①③④⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com