
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
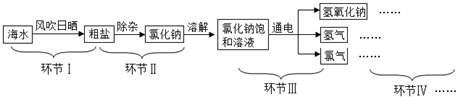
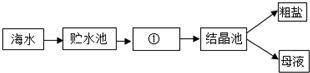
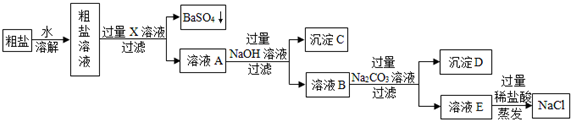
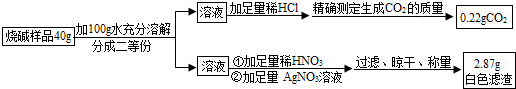
查看答案和解析>>
科目: 来源: 题型:解答题
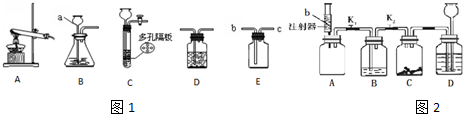
查看答案和解析>>
科目: 来源: 题型:解答题
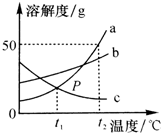 如图是a、b、c三种物质的溶解度曲线,回答下列问题:
如图是a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 有良好的导电性、导热性 | B. | 密度较大,熔点较低 | ||
| C. | 是银白色的固体 | D. | 都是混合物 |
查看答案和解析>>
科目: 来源: 题型:填空题
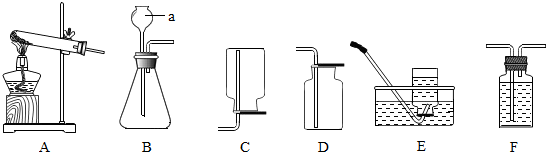
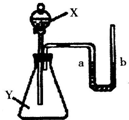 如下装置中,在密闭的锥形瓶中放入一种Y物质,当向分液漏斗中X物质滴入锥形瓶中时,U型管左侧液面下降,右侧液面上升,根据要求回答下列问题:
如下装置中,在密闭的锥形瓶中放入一种Y物质,当向分液漏斗中X物质滴入锥形瓶中时,U型管左侧液面下降,右侧液面上升,根据要求回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2SiO4 | B. | SiO2 | C. | Si | D. | SiH4 |
查看答案和解析>>
科目: 来源: 题型:解答题
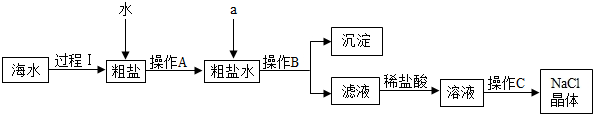
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
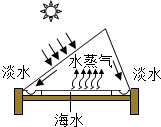 钓鱼岛及其附属岛屿自古以来就是我国固有领土,其附近海域蕴含丰富的化石燃料和矿产资源.
钓鱼岛及其附属岛屿自古以来就是我国固有领土,其附近海域蕴含丰富的化石燃料和矿产资源.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com