
科目: 来源: 题型:解答题
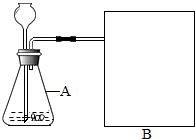 研究性学习小组选择“过氧化氢生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“过氧化氢生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:| 试验编号 | 1 | 2 |
| 反应物 | 6%的过氧化氢 | 6%的过氧化氢 |
| 催化剂 | 1g红砖粉 | 1g二氧化锰 |
| 时间 | 152s | 35s |
查看答案和解析>>
科目: 来源: 题型:解答题
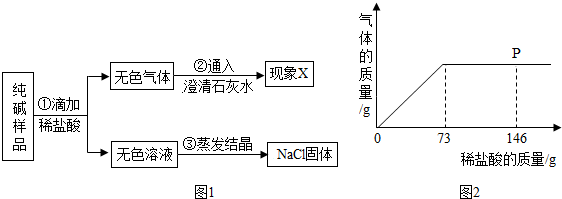
查看答案和解析>>
科目: 来源: 题型:解答题
| 气体制备仪器 | 气体性质仪器 |
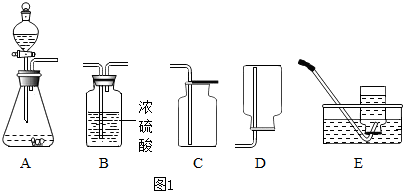 | 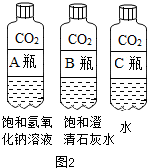 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
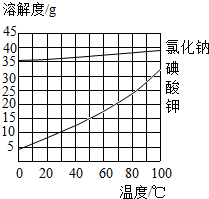 “食盐加碘”通常是在氯化钠中加入碘酸钾.如图是氯化钠和碘酸钾的溶解度曲线图.下列说法错误的是( )
“食盐加碘”通常是在氯化钠中加入碘酸钾.如图是氯化钠和碘酸钾的溶解度曲线图.下列说法错误的是( )| A. | 氯化钠易溶于水 | |
| B. | 碘酸钾的溶解度随温度升高而增大 | |
| C. | 20℃时不可能制得相同质量分数的碘酸钾溶液和氯化钠溶液 | |
| D. | 20℃时两者的饱和溶液,氯化钠的质量分数大 |
查看答案和解析>>
科目: 来源: 题型:选择题
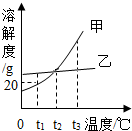 根据如图的溶解度曲线,判断下列说法不正确的是( )
根据如图的溶解度曲线,判断下列说法不正确的是( )| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | t1℃时甲物质的饱和溶液中溶质质量分数为20% | |
| C. | 将t2℃时乙物质的饱和溶液降到t1℃,有晶体析出 | |
| D. | t3℃时甲物质的溶解度大于t2℃时乙物质的溶解度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com