
科目: 来源: 题型:选择题
| A. | 常见的酸溶液:H2O、HCl、H2SO | B. | 常见的黑色固体:CuO、MnO2、Fe3O4 | ||
| C. | 常见的有还原性的物质:C、CO、O2 | D. | 常见的氧化物:MgO、KMnO4、H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
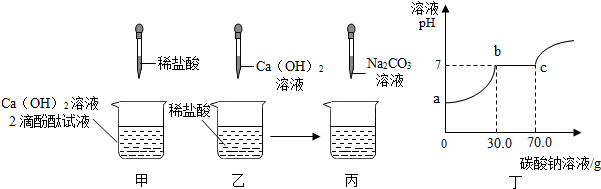
查看答案和解析>>
科目: 来源: 题型:解答题
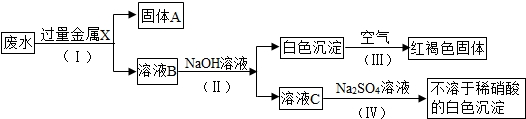
查看答案和解析>>
科目: 来源: 题型:解答题
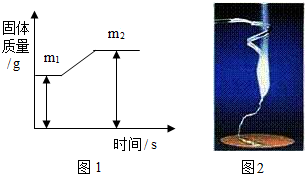 质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 白色粉末中可能有氯化钠和碳酸钙 | |
| B. | 白色粉末中肯定没有氢氧化钠和碳酸氢铵,可能有氯化钠 | |
| C. | 白色粉末中肯定有氯化钡、氢氧化钠、无水硫酸铜和碳酸钙 | |
| D. | 白色粉末中肯定有氢氧化钠和无水硫酸铜,且二者的质量比一定为1:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | “富氧空气”中氧气含量高于普通空气,其中氧气与其他气体体积比为21:79 | |
| B. | 铁丝在空气中能剧烈燃烧,火星四射,生成四氧化三铁 | |
| C. | 香肠采用真空包装的主要目的是为了隔绝水蒸气 | |
| D. | 从空气中分离出的氮气可用作食品防腐剂 |
查看答案和解析>>
科目: 来源: 题型:解答题
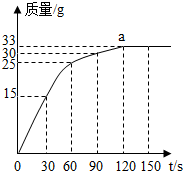 长期使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用酸溶液可以清除水垢.某初三同学学了酸的化学性质后通过实验来测定水垢中碳酸钙的含量:将足量的稀盐酸加入到100g水垢样品中,将产生的二氧化碳气体完全通入NaOH溶液中吸收,氢氧化钠溶液增加的质量随时间变化关系如图所示.
长期使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用酸溶液可以清除水垢.某初三同学学了酸的化学性质后通过实验来测定水垢中碳酸钙的含量:将足量的稀盐酸加入到100g水垢样品中,将产生的二氧化碳气体完全通入NaOH溶液中吸收,氢氧化钠溶液增加的质量随时间变化关系如图所示.查看答案和解析>>
科目: 来源: 题型:解答题

 “为铜片):实验较长时间后.发现D试管中铜片最先生锈(填试管字母编号).
“为铜片):实验较长时间后.发现D试管中铜片最先生锈(填试管字母编号).查看答案和解析>>
科目: 来源: 题型:解答题
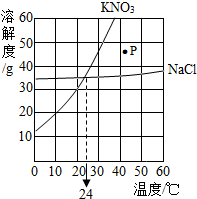 图为硝酸钾和氯化钠的溶解度曲线.由图可知:
图为硝酸钾和氯化钠的溶解度曲线.由图可知:查看答案和解析>>
科目: 来源: 题型:解答题
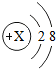 如图是某粒子的结构示意图,回答下列问题:
如图是某粒子的结构示意图,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com