
科目: 来源: 题型:选择题
| A. | CaO+H2O→Ca(OH)2 | B. | 2H2O→2H2↑+O2↑ | ||
| C. | 4Fe+3O2$\stackrel{点燃}{→}$2Fe2O3 | D. | Zn+HCl→ZnCl2+H2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
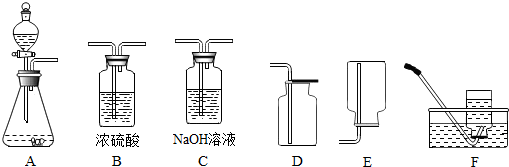
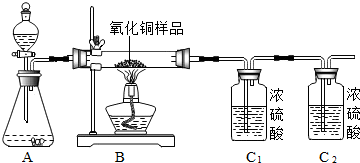
| 装置B中固体质量 | 装置C1的质量 | |
| 反应前 | 10.0克 | 150.8克 |
| 反应后 | 8.4克 | 152.8克 |
查看答案和解析>>
科目: 来源: 题型:解答题
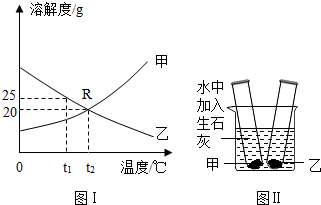
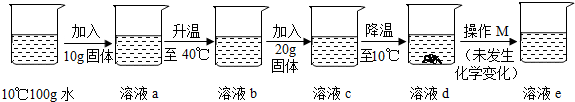
查看答案和解析>>
科目: 来源: 题型:解答题
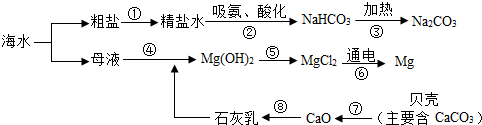

查看答案和解析>>
科目: 来源: 题型:选择题
| 待鉴别的物质 | 方案设计一 | 方案设计二 | |
| A | 铜片和黄铜片(铜锌合金) | 相互刻划,比较硬度. | 加入稀硫酸,观察现象. |
| B | 铁粉和氧化铜粉末 | 分别加入适量稀盐酸, 观察现象. | 分别加入硫酸铜溶液,观察现象. |
| C | K2CO3和NH4HCO3 | 分别加入熟石灰研磨,闻气味. | 分别加热,闻气味. |
| D | 甲烷和CO气体 | 分别点燃,火焰上方各罩一只 干冷烧杯,观察现象. | 分别通入澄清石灰水, 观察现象. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
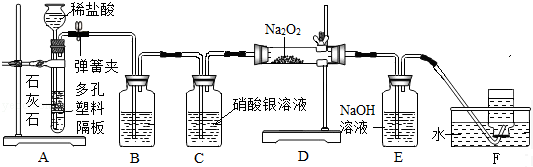
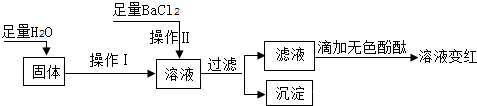
查看答案和解析>>
科目: 来源: 题型:解答题
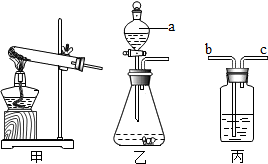
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com