
科目: 来源: 题型:实验探究题
 为了研究反应中压强的变化情况,利用如图进行实验.
为了研究反应中压强的变化情况,利用如图进行实验.查看答案和解析>>
科目: 来源: 题型:实验探究题
 化学小组同学用如图所示装置探究铁的金属活动性.
化学小组同学用如图所示装置探究铁的金属活动性.查看答案和解析>>
科目: 来源: 题型:实验探究题
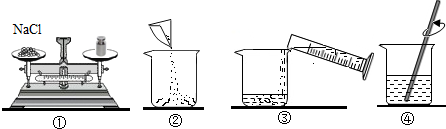
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题
 纯碱是一种重要的化工原料,广泛应用于玻璃、造纸、纺织和洗涤剂的生产.
纯碱是一种重要的化工原料,广泛应用于玻璃、造纸、纺织和洗涤剂的生产. 所示.该气体遇空气中的水蒸气易形成酸雾,腐蚀金属设备.该酸雾腐蚀金属铁的化学方程式为Fe+2HCl═FeCl2+H2↑.
所示.该气体遇空气中的水蒸气易形成酸雾,腐蚀金属设备.该酸雾腐蚀金属铁的化学方程式为Fe+2HCl═FeCl2+H2↑.查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
 他们到达了露营目的地.
他们到达了露营目的地.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NH4NO2由三种元素组成 | |
| B. | 反应①为复分解反应,反应②为分解反应 | |
| C. | 利用 NH4Cl 处理NaNO2最终转化为NaCl、N2和H2O | |
| D. | 上述反应所涉及的物质中,氮元素的化合价有四种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com