
科目: 来源: 题型:解答题
 下列是初中常见物质,由下表中元素组成.
下列是初中常见物质,由下表中元素组成.| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 铁 |
| 元素符号 | H | C | O | Cl | Na | Fe |
查看答案和解析>>
科目: 来源: 题型:解答题
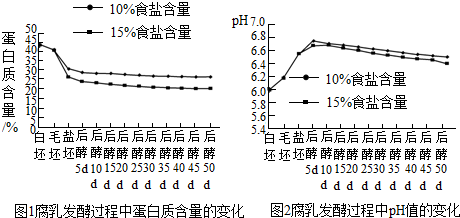
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别碳酸钠溶液和氯化钠溶液 | 取样,滴加酚酞溶液 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 证明NaOH溶液变质 | 取样,滴加盐酸,将生成气体 通入石灰水 |
| D | 探究Mg、Ag、Cu金属的 活动性顺序 | 将两根光亮的镁条分别伸入 硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
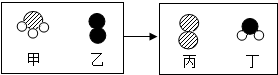 化学式在原子、分子水平上研究物质及其变化的科学.
化学式在原子、分子水平上研究物质及其变化的科学.| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2、OH-、CO32- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该固体样品中一定含有碳酸钾 | |
| B. | 该固体样品中一定含有碳酸钠和硝酸钠 | |
| C. | 该固体样品中可能含有硝酸钠和硝酸钡 | |
| D. | 加足量的水溶解得无色溶液,说明样品中一定没有硫酸铜 |
查看答案和解析>>
科目: 来源: 题型:解答题
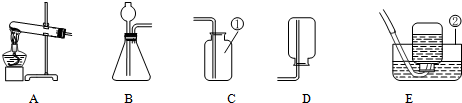
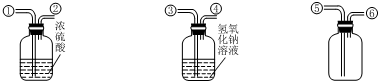
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com