4.“水循环”、“氧循环”和“碳循环”是自然界存在的三大重要循环.结合你所学到的化学知识回答下面有关问题.
(1)从物质变化的角度看,三大循环中有一种变化与另外两种变化有本质的区别,这一循环是水循环,这种循环主要是由水分子 的运动引起的.
(2)从微观角度看,水分子是由氢原子、氧原子构成的;从宏观角度看,二氧化碳是由碳元素和氧元素 组成的.
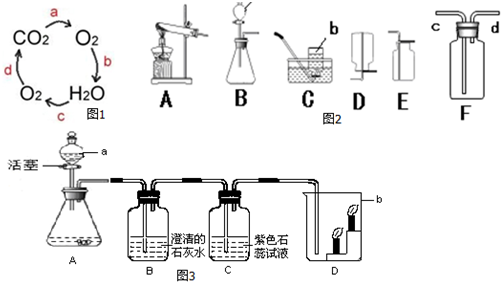
(3)如图1表示水、二氧化碳和氧气的循环图.
①图中a是自然界中消耗二氧化碳的主要途径,其名称为光合作用.
除此以外,自然界中消耗二氧化碳的另一主要途径为海水吸收,此过程发生反应的化学方程式为:CO
2+H
2O=H
2CO
3②请各举一例实现图中所示的物质变化,写出有关反应的化学方程式.
变化b化学方程式2H
2+O
2$\frac{\underline{\;点燃\;}}{\;}$2H
2O 变化c化学方程式2H
2O$\frac{\underline{\;通电\;}}{\;}$2H
2↑+O
2↑
变化d化学方程式C+O
2$\frac{\underline{\;点燃\;}}{\;}$CO
2(4)在刚刚结束的“两会”上提出:今年二氧化碳排放强度要降低3.1%以上,二氧化硫、氮氧化物排放要分别减少3%左右和5%左右.请回答下列问题:
①现行空气质量日报中,未计入空气污染指数项目的是:A(填序号)
A.二氧化碳 B.二氧化硫 C.氮氧化物 D.可吸入颗粒物 E.臭氧
②大气中的CO
2含量不断上升引起的环境问题是温室效应
大气中的CO
2是不是越少越好?为什么?不是,因为植物的光合作用需要氧气(或二氧化碳太少,地表生物将遭受强烈紫外线的伤害,甚至地球也可能会变成冰球等)
③人类降低空气中CO
2含量的两个研究方向:一是增强对CO
2的吸收,别一个是减少排放.“低碳经济”是一种以低能耗和高效能等为主要特征,以较少的二氧化碳排放获得较大产出的新经济发展模式.下列做法中不符合“低碳经济”理念的是B(填序号)
A.为了节约用纸,两面使用草稿纸
B.为了“QQ”能够升级,长期把“QQ”挂在线上
C.减少使用私加车次数,多乘公交车、骑自行车或步行
D.开发新能源,逐渐取缔直接利用化石燃料的历史
(5)研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们被为一种潜在的清洁燃料.
①在实验室中为探究氨气的性质,常用碱石灰和硫酸铵两种固体混合加热的方法制取氨气.通常情况下,氨气是一种极易溶于水,密度比空气小的气体.
请回答下列问题:
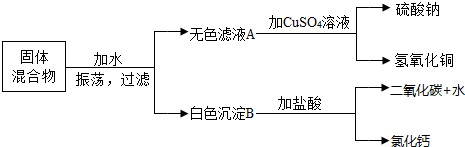
实验室制取氨气时发生装置A(填字母序号,下同)在C、D、E 三种装置中,收集氨气应选择D 若用装置F 收集氨 气,则应将d(填如图2“c”或”d”)与发生装置相连接.
②如图3是实验室用石灰石与稀盐酸反应制取二氧化碳并验证其性质的实验装置图,试根据题目要求回答下列问题:
实验开始前,应检查装置A的气密性,方法是:关闭活塞,将导管一端浸在水中,双手紧捂锥形瓶,有气泡冒出,说明气密性良好
装置A中发生的化学方程式为CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
装置B中观察到的现象是石灰水变浑浊化学方程式为Ca(OH)
2+CO
2=CaCO
3↓+H
2O
装置C中观察到的现象是石蕊变红色,发生反应的化学方程式为CO
2+H
2O=H
2CO
3装置D中观察到的现象是下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有不燃烧不支持燃烧、密度比空气大的性质.由此可知,二氧化碳在生活中可用于灭火.

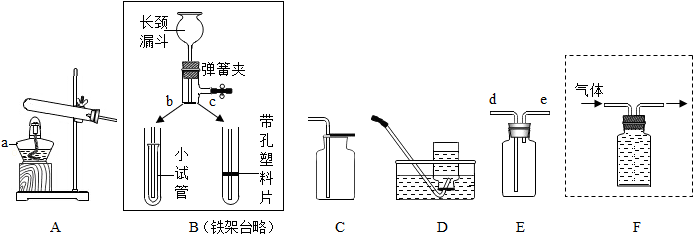

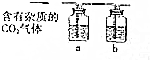 化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.
化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.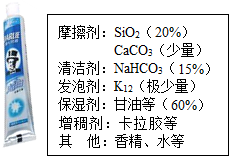 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏(如右图)展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏(如右图)展开如下探究,请回答问题: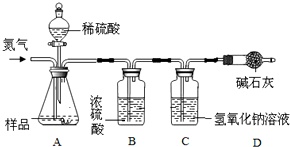
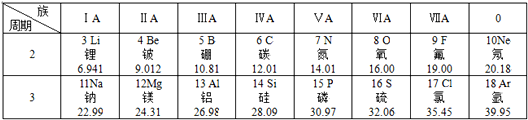
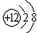 .该元素的原子核外有3个电子层,它属于元素金属(填“金属”、“非金属”).
.该元素的原子核外有3个电子层,它属于元素金属(填“金属”、“非金属”). 长期使用的热水壶底部有一层水垢(主要成分是碳酸鈣和氢氧化镁,现假定不含其它杂质).为了测定水垢中碳酸钙的含量,将足量质量分数为10.0%的盐酸加入到12.0g水垢中,产生CO2气体的情况如图所示.
长期使用的热水壶底部有一层水垢(主要成分是碳酸鈣和氢氧化镁,现假定不含其它杂质).为了测定水垢中碳酸钙的含量,将足量质量分数为10.0%的盐酸加入到12.0g水垢中,产生CO2气体的情况如图所示.