
科目: 来源: 题型:选择题
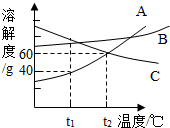 如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )
如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )| A. | t2℃时,A和C的饱和溶液中溶质的质量分数相等 | |
| B. | t1℃时,100g水溶解了40gA就达到了饱和状态 | |
| C. | A的溶解度大于C的溶解度溶质的质量分数相等 | |
| D. | A和B的饱和溶液从t2℃降到t1℃时,溶液的溶质质量分数都变小 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
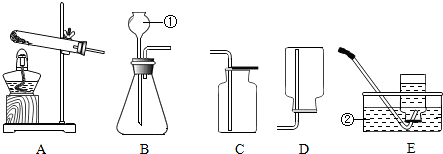
| 选项 | A | B | C |
| 试剂 | NaOH溶液 | CuO固体 | 浓硫酸 |
| 部分 装置 |  | 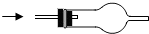 | 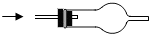 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
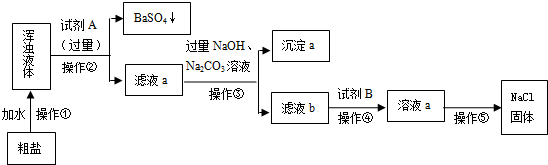
查看答案和解析>>
科目: 来源: 题型:填空题
 如图所示,是A、B、C三种固体物质的溶解度曲线.
如图所示,是A、B、C三种固体物质的溶解度曲线.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
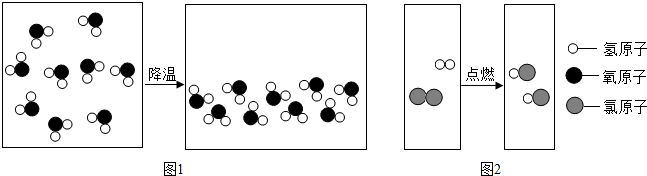
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com