
科目: 来源: 题型:选择题
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Mg2+ | |
| C. | 滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+ | |
| D. | 滤纸上有Ag、Cu、Zn、Mg,滤液中有Mg2+ |
查看答案和解析>>
科目: 来源: 题型:选择题
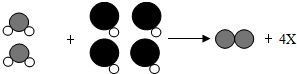 如图为某反应的微观示意图,其中不同的球代表不同元素的原子.下列说法正确的是( )
如图为某反应的微观示意图,其中不同的球代表不同元素的原子.下列说法正确的是( )| A. | 1个X分子中有3个原子 | |
| B. | 该反应属于置换反应 | |
| C. | 反应物分子的个数比为1:1 | |
| D. | 黑球表示的元素化合价在反应前后未改变 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | O2和O3的分子构成不同,所以它们的化学性质不同 | |
| B. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 因为酸溶液呈酸性,所以呈酸性的溶液一定是酸溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向试管里倾倒液体时,试剂瓶口要紧挨试管口 | |
| B. | 用滴管滴加液体时,滴管不能触及容器的内壁 | |
| C. | 为节约火柴,用燃着的酒精灯引燃其他酒精灯 | |
| D. | 用量筒量取液体时,视线要与量筒内液体的凹液面的最低处保持水平 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 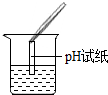 | 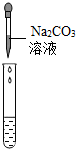 | 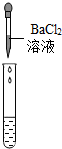 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
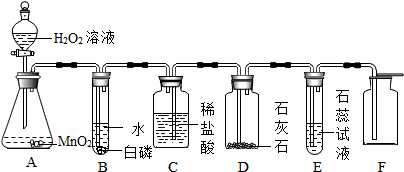
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
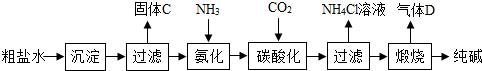
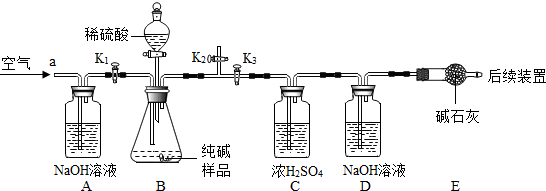
查看答案和解析>>
科目: 来源: 题型:实验探究题
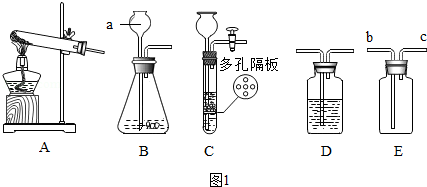
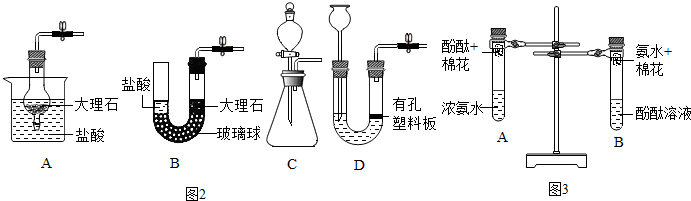
查看答案和解析>>
科目: 来源: 题型:实验探究题
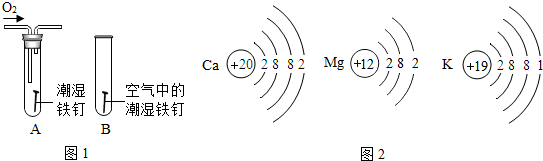
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com