
科目: 来源: 题型:填空题
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去铜粉中含有的少量铁粉 | 将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥 |
| B | 鉴别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液 | 不用其它任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③② |
| C | 除去CO2中的少量HCl气体 | 通过Na2CO3溶液,再通过浓硫酸 |
| D | 鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,观察现象 |
查看答案和解析>>
科目: 来源: 题型:解答题
 实验室有一瓶久置的浓盐酸,部分标签如图所示,为了确定该溶液中HCl的含量,某化学兴趣小组做了以下实验:取20g该溶液于烧杯中加入CuO固体,至刚好不溶解时,加入的固体质量为4g.
实验室有一瓶久置的浓盐酸,部分标签如图所示,为了确定该溶液中HCl的含量,某化学兴趣小组做了以下实验:取20g该溶液于烧杯中加入CuO固体,至刚好不溶解时,加入的固体质量为4g.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
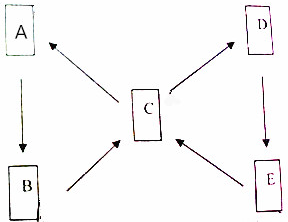 A、B、C、D、E都是含铜元素的物质,其中,A为单质,其它都是铜的化合物且铜元素在这些化合物中都显+2价,B为黑色物质,C为一种硫酸盐且为蓝色溶液,D和胃液中的酸含有一种相同的元素,E为蓝色沉淀,它们的转化关系如图所示,请你结合信息推断:
A、B、C、D、E都是含铜元素的物质,其中,A为单质,其它都是铜的化合物且铜元素在这些化合物中都显+2价,B为黑色物质,C为一种硫酸盐且为蓝色溶液,D和胃液中的酸含有一种相同的元素,E为蓝色沉淀,它们的转化关系如图所示,请你结合信息推断:查看答案和解析>>
科目: 来源: 题型:实验探究题
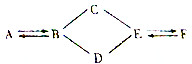 如图A、B、C、D、E、F是切中化学常见的物质,且A、B、C、D、E属于不同类别的物质,C的水溶液呈蓝色,B是年产量最高的金属,A→B的反应可用于冶金工业,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)
如图A、B、C、D、E、F是切中化学常见的物质,且A、B、C、D、E属于不同类别的物质,C的水溶液呈蓝色,B是年产量最高的金属,A→B的反应可用于冶金工业,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)查看答案和解析>>
科目: 来源: 题型:实验探究题
 已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.
已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一氧化碳和二氧化碳的化学性质不同-分子的构成不同 | |
| B. | 硫和磷的元素种类不同-质子数不同 | |
| C. | 金刚石和石墨的物理性质不同-组成元素不同 | |
| D. | 硫在空气中燃烧的火焰颜色不同-氧气浓度不同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 复合材料:玻璃钢、钢筋混凝土 | B. | 碱:烧碱、纯碱 | ||
| C. | 盐:氯化钾、氯化氢 | D. | 合金:金、青铜 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取样逐滴滴加稀盐酸 | 开始时无明显现象,过一段时间后有大量气泡产生 | 该瓶氢氧化钠溶液部分(填“全部”或“部分”)变质,滴加稀盐酸后发生反应的化学方程式:①aOH+HCl=NaCl+H2O、②Na2CO3+2HCl=2NaCl+CO2↑+H2O |

查看答案和解析>>
科目: 来源: 题型:解答题
 向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入稀盐酸的质量与产生气体的关系如图:
向盛有22.3g Na2CO3和NaCl固体混合物的烧杯中加入稀盐酸的质量与产生气体的关系如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com