
科目: 来源: 题型:选择题
| A. | 用碳酸氢钠作发酵粉 | |
| B. | 工业酒精也可以饮用 | |
| C. | 用霉变油菜籽生产食用油 | |
| D. | 食用用甲醛溶液浸泡过的海鲜对人体无害 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
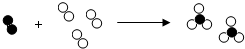 在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为
在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为 ,乙表示为
,乙表示为 ,丙表示为
,丙表示为 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 沸点不能太低 | B. | 沸点不能太高 | ||
| C. | 能通过减压来提高沸点 | D. | 不易挥发 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | PM2.5与雾霾天气 | B. | 新装修屋内的空气杀手 | ||
| C. | 酸雨的罪魁祸首 | D. | 室内燃气热水器的安全防范 |
查看答案和解析>>
科目: 来源: 题型:推断题


查看答案和解析>>
科目: 来源: 题型:解答题
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/ml | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/ml | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:选择题
 淀粉酶可以将人体不能直接吸收的淀粉转变成易吸收的小分子物质,如图是淀粉酶对淀粉作用过程的示意图.下列对该过程的表述中,错误的是( )
淀粉酶可以将人体不能直接吸收的淀粉转变成易吸收的小分子物质,如图是淀粉酶对淀粉作用过程的示意图.下列对该过程的表述中,错误的是( )| A. | 是物理变化 | B. | 是化学变化 | ||
| C. | 酶起催化作用 | D. | 酶的化学性质没有改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com