
科目: 来源: 题型:选择题
| A. | X由碳、氢、氧三种元素组成 | B. | 检验X用燃着的木条 | ||
| C. | X中碳、氧元素的质量比为3:4 | D. | X中碳、氧元素的化合价代数和为零 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 操作步骤 | 1.取三支试管,分别加入a、b、c三种溶液 2.用胶头滴管往三支试管中分别滴加d溶液 | ||
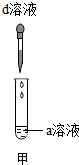 | 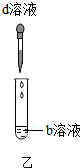 | 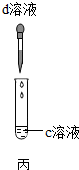 | |
| 魔术名称 | 变红酒 | 变汽水 | 变牛奶 |
| 现象 | 溶液呈红色 | 产生大量气泡 | 出现白色沉淀 |
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液与试管中,加入碳酸钠溶液 | 有白色沉淀生成 | 猜想正确 |
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
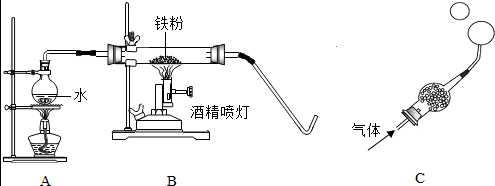
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
| 实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 若固体全部溶解,没有气泡冒出,则猜想二正确;若固体全部溶解,有气泡冒出,则猜想一正确. |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 序号 | 5%过氧化氢溶液 | 其他物质 | 加热的温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | 330℃ | 100mL | t1 | |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | t2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | t3 |
| ④ | 2.0g | MnO20.5 g | 380℃ | 100mL | t4 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验编号 | 硫酸的质量分数(均取200mL) | 锌的颗粒大小(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌粉 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌粉 | 75.4 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| 氢气的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
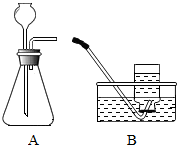 某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.
某研究性学习小组在探究“锌与硫酸反应快慢的影响因素”时,发现一个意外现象:硫酸中混有硫酸铜溶液时,产生氢气的速率更快.| 编号 | 20%的稀硫酸各20mL | 锌粒 | 收集1瓶氢气所需的时间 |
| ① | 加入质量分数为10%的硫酸铜溶液1mL | 1g | 2分10秒 |
| ② | 加入质量分数为10%的硫酸锌溶液1mL | 1g | 3分01秒 |
| 编号 | 实验步骤 | 实验现象比较 | 实验结论 |
| ① | 取1g锌粒于锥形瓶中, 加入20mL 20%的稀硫酸 | 产生氢气的速率较快与铜单质有关 | |
| ② |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com