
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:填空题
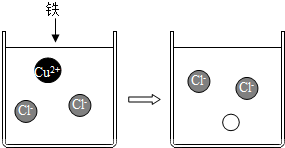 含有相同离子的盐具有相似的性质.
含有相同离子的盐具有相似的性质. ”代表的离子符号Fe2+.
”代表的离子符号Fe2+.查看答案和解析>>
科目: 来源: 题型:实验探究题
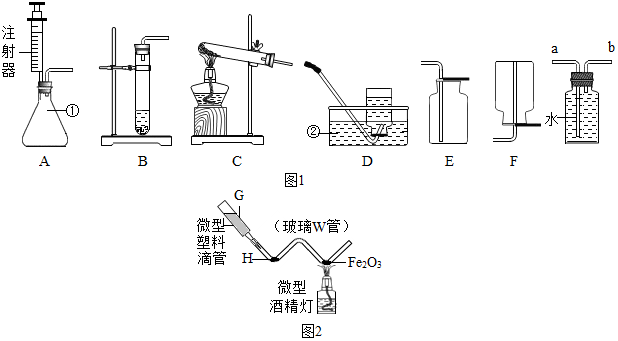
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
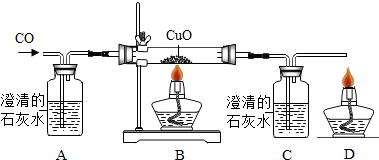

| 序号 | 样 品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1.0g铁粉、0.2g碳和10滴水 | 100 | 75.4 | 约120 |
| ② | 1.0g铁粉、0.2g碳和10滴水和少量NaCl | 100 | 75.4 | 约70 |
| ③ | 1g铁粉、10滴水 | / | / | / |
查看答案和解析>>
科目: 来源: 题型:实验探究题
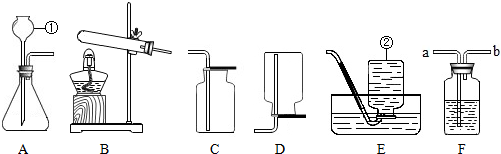
查看答案和解析>>
科目: 来源: 题型:解答题
 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:
为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量/g | 氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
查看答案和解析>>
科目: 来源: 题型:推断题
 有A、B、C、D、E、F、G、H初中常见的八种物质,A与B的组成元素相同,D和 G组成元素相同.A中只含两种元素且质量比为1:16,F为紫红色.八种物质之间有如图转化关系,部分反应物、生成物及反应条件略去,请回答:
有A、B、C、D、E、F、G、H初中常见的八种物质,A与B的组成元素相同,D和 G组成元素相同.A中只含两种元素且质量比为1:16,F为紫红色.八种物质之间有如图转化关系,部分反应物、生成物及反应条件略去,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com