
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验探究题
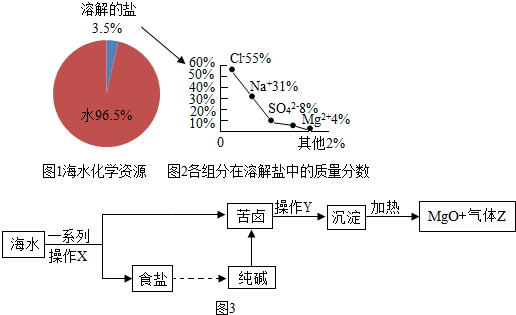
查看答案和解析>>
科目: 来源: 题型:实验探究题
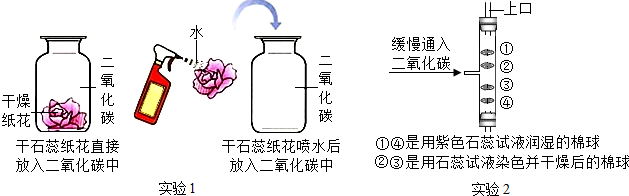
查看答案和解析>>
科目: 来源: 题型:填空题
| 项目 | 能量 | 蛋白质 | 脂肪 | 糖类 | 钠 |
| 每100g | 329kJ | 2.6g | 3.1g | 10.0g | 60mg |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHCO3是纯碱 | |
| B. | 析出晶体后剩余溶液中溶质只有NH4Cl | |
| C. | 配制饱和食盐水时,可通过搅拌来提高食盐的溶解度 | |
| D. | 向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收 |
查看答案和解析>>
科目: 来源: 题型:推断题
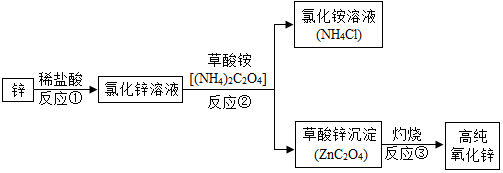
查看答案和解析>>
科目: 来源: 题型:解答题
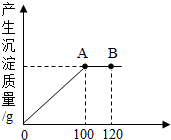 管理员在学校实验室发现了一瓶敞口放置的氢氧化钠溶液,同学小晴认为该溶液已部分变质成Na2CO3,为探究溶液中溶质的成分,请回答下列问题.
管理员在学校实验室发现了一瓶敞口放置的氢氧化钠溶液,同学小晴认为该溶液已部分变质成Na2CO3,为探究溶液中溶质的成分,请回答下列问题.查看答案和解析>>
科目: 来源: 题型:实验探究题
 有一固体混合物A,己知其中可能含有NH4N03、NaCl、CuS04、BaC03,Fe(N03)3五种物质中的两种或多种,按下列步骤所示进行实验(设过程中所有发生的反应都恰好完全进行).
有一固体混合物A,己知其中可能含有NH4N03、NaCl、CuS04、BaC03,Fe(N03)3五种物质中的两种或多种,按下列步骤所示进行实验(设过程中所有发生的反应都恰好完全进行).查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
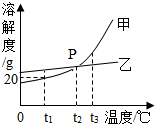 甲、乙两种不含结晶水的固体物质的溶解度曲线如图:
甲、乙两种不含结晶水的固体物质的溶解度曲线如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com