
科目: 来源: 题型:解答题
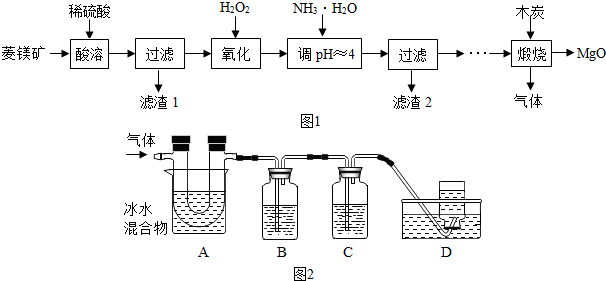
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

| 实验人员 | 红色固体(g) | 剩余红色固体(g) | 实验结论 |
| 甲 | 7.2 | 3.2 | 假设二成立 |
| 乙 | 4.08 | 2.48 | 假设三成立 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 空气是一种宝贵的资源 | |
| B. | 氧气可用作火箭发射的燃料 | |
| C. | 相比空气,“人造空气”中的氮气含量低 | |
| D. | 燃烧和缓慢氧化都属于氧化反应 |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
 某化学兴趣小组的同学要利用课余时间,在实验室进行一些力所能及的探究活动,请你参加并协助他们完成部分探究任务.
某化学兴趣小组的同学要利用课余时间,在实验室进行一些力所能及的探究活动,请你参加并协助他们完成部分探究任务.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 甲实验的步骤是①④⑤,其中除杂质的关键步骤是蒸发 | |
| B. | 甲实验④中,玻璃棒的作用是搅拌加快过滤速度 | |
| C. | 乙实验若按②③①的步骤进行操作,所配溶液的浓度会偏小(水的密度为1g/cm3) | |
| D. | 乙实验②中,若左盘放砝码,右盘放药品,所称得的氯化钠一定比实际需要量少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com