
科目: 来源: 题型:实验探究题
| 实验一 | 实验二 |
 |  |
| 实验三 | 实验四 |
 |  |
| 实验五 | |
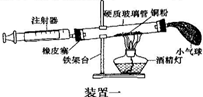 |  |
| 硬质玻璃管 的容积 | 反应前注射器中 气体体积 | 反应后注射器中气体体积 | 实验测得空气中氧气 的体积分数 |
| 30mL | 20mL | 12mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 实行垃圾分类回收再利用 | B. | 控制烟花爆竹的燃放 | ||
| C. | 推广秸秆综合利用杜绝露天焚烧 | D. | 过量使用农药化肥提高农作物产量 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
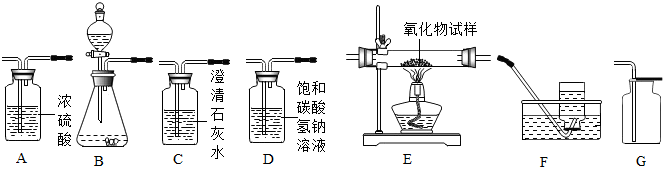
查看答案和解析>>
科目: 来源: 题型:解答题
 水是一种重要的资源.
水是一种重要的资源.| 石蕊试液 | 氯化钡溶液 | |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
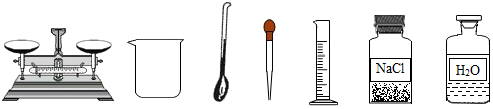
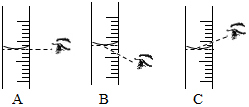
查看答案和解析>>
科目: 来源: 题型:解答题
 在哈尔滨市继今年1月份5台纯电动公交车上道试运营后,近日两台插电式气电混合动力公交车也在公交8路、107路上线试运营.插电式混合动力公交车车速23公里/小时以下,为纯电力驱动;速度超过23公里/小时,为气电混合驱动.按照测算,与常规天然气公交车相比,氮氧化物排放量可减少76%、二氧化碳排放量可减少60%,PM排放量可减少86%.回答下列问题.
在哈尔滨市继今年1月份5台纯电动公交车上道试运营后,近日两台插电式气电混合动力公交车也在公交8路、107路上线试运营.插电式混合动力公交车车速23公里/小时以下,为纯电力驱动;速度超过23公里/小时,为气电混合驱动.按照测算,与常规天然气公交车相比,氮氧化物排放量可减少76%、二氧化碳排放量可减少60%,PM排放量可减少86%.回答下列问题.查看答案和解析>>
科目: 来源: 题型:选择题
 哈尔滨地铁是中国首个高寒地铁系统,规划“九线一环”,总里程340公里,有10条规划线路.下列有关叙述错误的是( )
哈尔滨地铁是中国首个高寒地铁系统,规划“九线一环”,总里程340公里,有10条规划线路.下列有关叙述错误的是( )| A. | 地铁的使用,有效缓解了主城区的交通压力 | |
| B. | 地铁车厢外部的喷漆起到既防锈又美观的作用 | |
| C. | 地铁的钢轨采用了锰钢,具有硬度大、韧性好的性能 | |
| D. | 地铁施工过程中使用了大量的合成材料,如钢筋混凝土等,使工程更加坚固 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一氧化碳和氧化铜在高温下反应,生成红色的铜 | |
| B. | 打开盛有浓盐酸的瓶盖,瓶口产生大量的白烟 | |
| C. | 电解水时,与正极相连的玻璃管内生成的气体能使带火星的木条复燃 | |
| D. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com