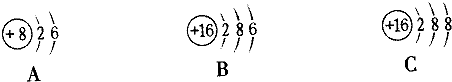
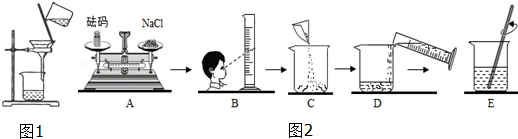
5.某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?他们就铜与浓硫酸是否能反应及相关问题进行了实验探究.
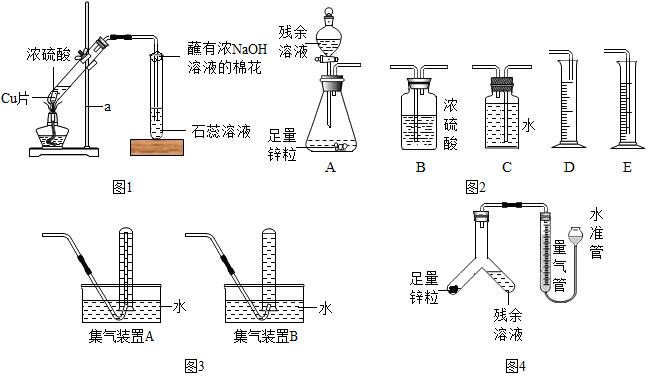
【探究一:铜与浓硫酸是否能反应?】
同学们设计了如图1所示装置进行探究.
①在常温下能反应;
②常温下不能反应,但在加热条件下能反应;
③在加热条件下不能反应;
操作①:连接仪器,检查装置气密性;
操作②:将过量的铜片放入试管中,加入浓硫酸,无明显现象;
操作③:加热该试管,铜片上有气泡,试管内溶液由无色变为蓝色,产生了有刺激性气味的气体;…
(1)写出仪器a的名称:铁架台;
(2)甲同学认为,由以上实验过程可知:猜想②(填序号)是正确的;
(3)可观察到试管中的石蕊试液变红.
乙同学认为,铜跟浓硫酸在加热条件下反应的产物只是SO
2和CuSO
4;
(4)丙同学认为,在实验装置中,“蘸有浓NaOH溶液棉花”的作用是吸收SO
2,写出相关反应的化学方程式2NaOH+SO
2═Na
2SO
3+H
2O.
(5)在(3)中对产物只是SO
2和CuSO
4的判断是否准确否(填“是”或“否”),其理由是反应物中有氢元素,但二氧化硫和硫酸铜中都不含氢元素.写出铜与浓硫酸在加热条件下反应的化学方程式Cu+2H
2SO
4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO
4+2H
2O+SO
2↑.
(6)根据以上探究和已掌握的知识,该兴趣小组的同学设计了两种用铜制取硫酸铜的实验方案:
方案一:Cu$→_{加热}^{浓硫酸}$CuSO
4 方案二:Cu$→_{加热}^{O_{2}}$CuO$\stackrel{稀硫酸}{→}$CuSO
4经过对两种方案的讨论、对比,同学们认为方案二具有的优点有BC(填序号),所以工业上制备硫酸铜不是直接利用浓硫酸与铜反应.
A.提高铜的利用率 B.提高硫酸的利用率 C.不产生污染大气的SO
2【探究二:测定反应残余清液中硫酸的溶质质量分数】
同学们对上述实验后试管内残余清液成分进行了讨论,过量的铜与浓硫酸在加热条件下反应不能将硫酸耗尽.为测定反应残余清液中硫酸的溶质质量分数,探究小组同学提出了下列实验方案:
:含杂质的锌与稀硫酸反应时比纯锌与稀硫酸反应更快,放出大量热
:甲方案:与足量BaCl
2溶液反应,称量生成的BaSO
4质量.
乙方案:与足量锌粒反应,测量生成氢气的体积.
回答下列问题:
(1)该反应中即使铜过量也不能将硫酸完全反应的原因是物质的化学性质除了与物质本身的性质有关,还可能和溶液中溶质的浓度有关;
(2)甲方案是否可行?不可行(填“可行”或“不可行”),理由是加入足量的BaCl
2溶液只能求出硫酸根离子的量,而不能求出剩余硫酸的浓度;
(3)小王同学选用图2中的部分实验装置进行了乙方案的实验:
①你认为图2中最简易的装置及其连接顺序是:ACE;
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,过一会儿后残余清液就不能顺利滴入锥形瓶.其原因是AB(填序号);
A.锌与硫酸铜反应生成了铜,不纯的锌与硫酸反应速率加快;
B.反应产生大量气体且放热,使瓶中压强增大;
③某学生想用排水法收集氢气并检验其纯度,应选择图3中的集气装置B (填“A”或“B”).
(4)小张同学用如图4所示装置进行了乙方案的实验
①连接仪器,检查此装置气密性.下列能说明装置气密性良好的是A(填序号);
A.连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差.
B.向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平.
②实验中使Y形管中的残余清液与锌粒反应的正确操作是倾斜,将锌粒(选填“锌粒”或“残余清液”)转移到Y形管的另一边.残余清液与锌粒混合后的现象是锌粒逐渐溶解、
表面析出暗红色固体、产生大量气泡,放出热量.
③反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变.气体体积逐渐减小的原因是反应是放热的,气体未冷却(排除仪器和实验操作的影响因素).
④该实验中残余清液质量为a g,测得生成气体体积为bmL(假设在实验条件下气体密度为cg/mL),残余清液中硫酸的溶质质量分数为$\frac{49bc}{a}×$100%(用含a、b、c的式子表示).
⑤若实验中测得残余清液中硫酸的溶质质量分数偏大,下列可能的原因是c.
a.装置漏气 b.读取数据时水准管的水面高于量气管的水面 c.未待冷却就读取量气管读数.