
科目: 来源: 题型:实验探究题
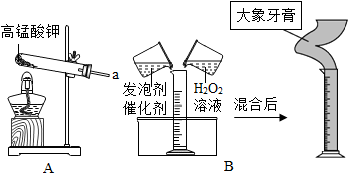
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HBr | B. | CaO | C. | Hg | D. | H2 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 甲 | 乙 | 丙 | |
| 样品质量/g | 25 | 30 | 25 |
| 稀硫酸质量/g | 120 | 80 | 80 |
| 充分反应后剩余物/g | 144.8 | 109.8 | 104.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验步骤及操作 | 实验现象 | 实验结论 |
| 取样于试管中,加入足量蒸馏水振荡,静置 ①取上层清液,滴入无色酚酞试液 ②倒去上层清液,再向试管中的残渣注入稀盐酸 | ①无色酚酞试液变红 ② | 部分变质 |
| ①无色酚酞试液不变红 ② | ||
| ①无色酚酞试液变红 ②没有气泡产生 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
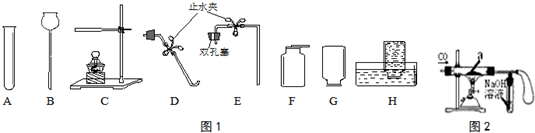
查看答案和解析>>
科目: 来源: 题型:推断题
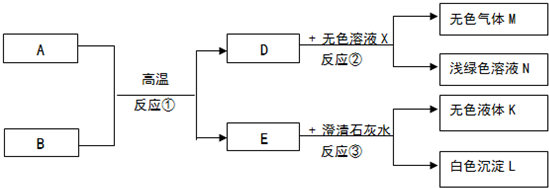
查看答案和解析>>
科目: 来源: 题型:实验探究题
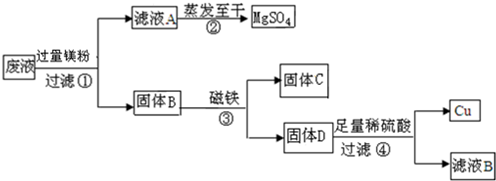
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com