
科目: 来源: 题型:选择题
| A. | 用澄清石灰水鉴别氢气和一氧化碳 | |
| B. | 用无色酚酞鉴别碳酸钠溶液和氢氧化钠溶液 | |
| C. | 用紫色石蕊溶液鉴别氯化铵溶液和稀盐酸 | |
| D. | 用水鉴别氢氧化钙固体和氢氧化钠固体 |
查看答案和解析>>
科目: 来源: 题型:推断题
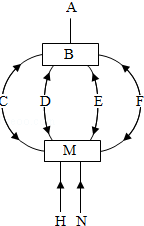 如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).
如图为九种物质的相互关系,其中A、B、C、M、N是氧化物,B常温下是液体,C是黑色固体,M、N为气体;H是固体单质,F常温下是固体,D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”表示转关系“-”表示反应关系(部分反应物、生成物和反应条件未标出).查看答案和解析>>
科目: 来源: 题型:推断题
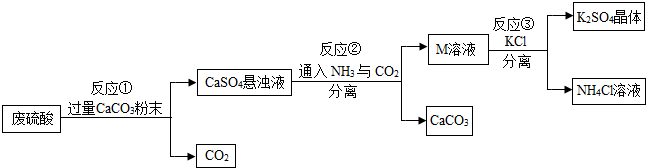
| 物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
实 验 内 容 |  |  |  |
| 实 验 现 象 | B(填字母编号) 瓶口的蓝色石蕊试纸很快变 红. | 两试管中均产生 气体 | 试管E:绿色粉末逐渐溶解,产生气泡,溶液显蓝色. 试管F:绿色粉末逐渐溶解,产生气泡,溶液显绿色. |
| 分 析 与 结 论 | 该酸有挥发性,另一种酸没有.不同的酸可能有不同的物理性质 | 不同的酸具有相似的化学性质,这是因为酸溶液中都含有H+(填符号). | 试管E中发生反应的化学方程式:Cu2(OH)2CO3+2H2SO4═ 2CuSO4+3H2O+CO2↑ 试管F中发生反应的化学方程式:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:推断题
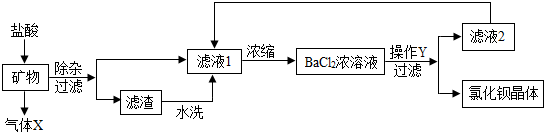
查看答案和解析>>
科目: 来源: 题型:填空题
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
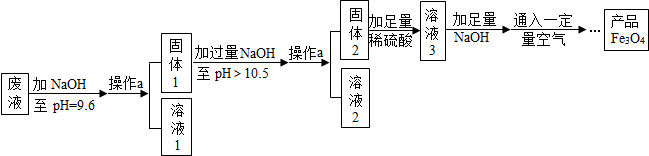
查看答案和解析>>
科目: 来源: 题型:解答题
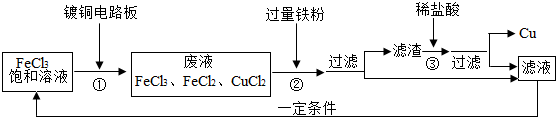
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:推断题
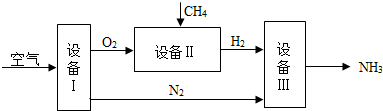
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 原混合气体中,H2的质量大于2g,同时氧气的质量小于16g | |
| B. | 原混合气体中,H2的质量大于2g,同时氧气的质量等于16g | |
| C. | 剩余的2g气体为N2 | |
| D. | 剩余的2g气体中含有H2、O2、N2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com