
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:实验探究题
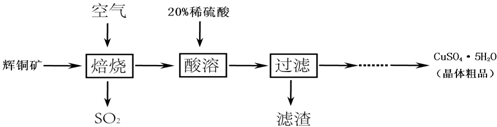
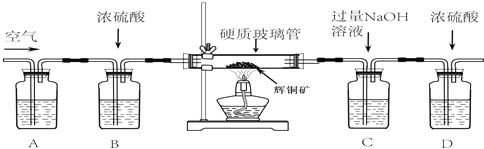
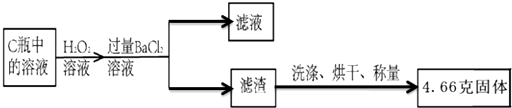
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题
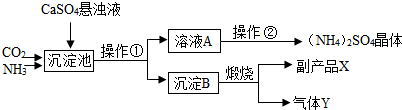
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 碳的相对原子质量为12.01 | B. | 氮原子的核外电子数为7 | ||
| C. | 氧元素只能形成一种单质 | D. | C、N、O的原子序数依次增加 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶液是均一、稳定的混合物 | |
| B. | 固体NaOH溶于水时,溶液温度升高 | |
| C. | 一定条件下,饱和溶液和不饱和溶液可以相互转化 | |
| D. | 溶液中的溶剂只能是水 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com