
科目: 来源: 题型:选择题
| A. | 用托盘天平称量固体时,应将药品放在右盘上,砝码放在左盘上 | |
| B. | 将试剂瓶中的液体倒入试管中,必须用漏斗引流 | |
| C. | 用排水法收集满氧气的集气瓶在水下用玻片盖好,再取出正立于桌面上 | |
| D. | 用10mL量筒准确量取了6.53mL水 |
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | +2 | B. | +4 | C. | +6 | D. | -2 |
查看答案和解析>>
科目: 来源: 题型:推断题
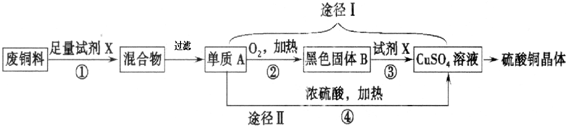
查看答案和解析>>
科目: 来源: 题型:推断题
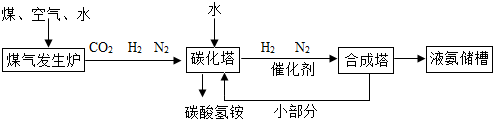
查看答案和解析>>
科目: 来源: 题型:推断题
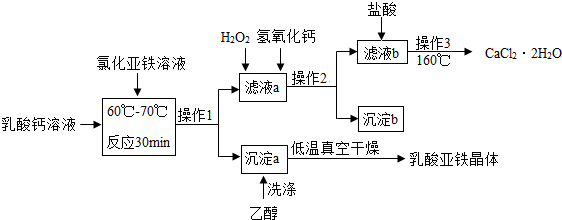
查看答案和解析>>
科目: 来源: 题型:解答题
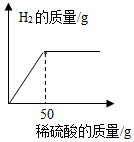 学校化学兴趣小组欲测定某含杂质的锌粒中锌的质量分数,小亮同学称取10g该样品加入到足量的稀硫酸中(杂质不溶于水也不与酸反应),测得一定时间内生成气体的质量如表所示:
学校化学兴趣小组欲测定某含杂质的锌粒中锌的质量分数,小亮同学称取10g该样品加入到足量的稀硫酸中(杂质不溶于水也不与酸反应),测得一定时间内生成气体的质量如表所示:| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| H2的质量(g) | 0.08 | 0.16 | 0.2 | 0.2 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com