
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验探究题
查看答案和解析>>
科目: 来源: 题型:实验探究题
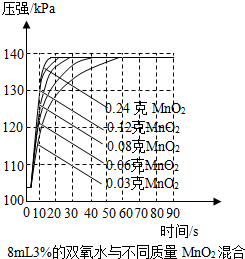 实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.
实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小王同学对“双氧水分解快慢的影响因素”进行了探究.| 实验编号 | 温度℃ | 二氧化锰的形状(均取0.4cm) | 收集到氧气的体积/mL(时间均为10s) |
| ① | 20 | 颗粒状 | a |
| ② | 30 | 粉末状 | b |
| ③ | 30 | 颗粒状 | c |
| ④ | 20 | 粉末状 | d |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(SO2) | 适量NaOH溶液 | 洗气 |
| B | K2SO4(KOH) | 适量HCl溶液 | 蒸发 |
| C | CO2(CO) | 足量O2 | 点燃 |
| D | FeCl2(CuCl2) | 足量铁屑 | 过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:实验探究题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 14.3 | 17.4 | 20.7 | 25 | 28.5 | 33.3 | 40 | 55 | 75.4 |


查看答案和解析>>
科目: 来源: 题型:实验探究题
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的pH | pH>7 | |
| CaCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com